Insulinresistenz: Symptome, Ursachen und therapeutische Ansätze
In den letzten Jahrzehnten ist die Häufigkeit von Stoffwechselstörungen – insbesondere Insulinresistenz (IR) und Typ-2-Diabetes mellitus (T2D) – weltweit dramatisch angestiegen. Dies ist vor allem auf die Urbanisierung, einen sitzenden Lebensstil und die Verbreitung kalorienreicher, westlicher Ernährungsweisen zurückzuführen. Insulinresistenz ist eine der häufigsten, aber oft übersehenen Stoffwechselstörungen; sie kann jahrelang latent vorhanden sein und dabei unbemerkt die Stoffwechselfunktionen des Körpers schädigen. Sie ist nicht nur eine Vorstufe von Typ-2-Diabetes, sondern trägt auch zu verschiedenen anderen Erkrankungen bei, darunter nichtalkoholische Fettlebererkrankungen (NAFLD), polyzystisches Ovarialsyndrom (PCOS) und Herz-Kreislauf-Erkrankungen. Neben traditionellen Risikofaktoren wie genetischer Veranlagung, übermäßiger Kalorienaufnahme und Bewegungsmangel weisen immer mehr Forschungsergebnisse auf die Bedeutung eines ausgeglichenen Darmmikrobiota hin. Die Zusammensetzung der Darmflora beeinflusst den Glukosestoffwechsel, chronische Low-Grade-Entzündungen und die Insulinsensitivität. Übergewicht – insbesondere viszerales Fett – erhöht das Risiko für T2D erheblich. Epidemiologische Daten zeigen, dass etwa 86 % der Menschen mit Typ-2-Diabetes übergewichtig oder fettleibig sind. Es muss jedoch betont werden, dass Übergewicht weder die einzige noch eine ausreichende Voraussetzung für die Entwicklung von Diabetes ist. Ob Übergewicht tatsächlich zu Diabetes führt, hängt weitgehend von der individuellen Insulinsensitivität, der Fettverteilung, der Hormonregulation und vor allem von der Funktion des Darmmikrobiota ab. Diabetes ist daher nicht nur eine Frage des Körpergewichts, sondern das Ergebnis komplexer, vielschichtiger metabolischer und immunologischer Wechselwirkungen. 1
Was ist Insulinresistenz?
Glukose ist eine lebenswichtige Energiequelle für den menschlichen Körper. Das Gehirn und viele Gewebe benötigen sie als Energiequelle, und rote Blutkörperchen, die für den Sauerstofftransport zuständig sind, können nur Glukose verwerten. Aufgrund ihrer chemischen Struktur ist Glukose sehr reaktiv und bindet sich leicht an Proteine, darunter auch solche in Blutgefäßen, Nervenzellen und roten Blutkörperchen. Diese Glykation kann die betroffenen Zellen schädigen und dazu führen, dass rote Blutkörperchen verklumpen, wodurch sie nur noch schwer durch die engen Kapillaren gelangen können und die Mikrozirkulation beeinträchtigt wird – insbesondere in empfindlichen Organen wie der Netzhaut und den Nieren. Der HbA1c-Wert, der in Labortests gemessen wird, gibt den Anteil an glykiertem Hämoglobin an und spiegelt damit wider, wie viel Zucker an das Hämoglobin in den roten Blutkörperchen gebunden ist. Der Blutzuckerspiegel wird streng reguliert, wobei Insulin eine zentrale Rolle spielt. Es ermöglicht Glukose aus dem Blutkreislauf in die Zellen zu gelangen, wo sie in Energie umgewandelt wird.
Über Insulin
Insulin wird von den Betazellen in den Langerhans-Inseln der Bauchspeicheldrüse produziert. Als Reaktion auf den Zucker in der Nahrung wird Insulin in den Blutkreislauf abgegeben. Es wirkt über Insulinrezeptoren auf bestimmte Zellen (z. B. Leber-, Muskel- und Fettzellen) und öffnet kleine Poren in der Zellmembran, durch die Glukose eindringen kann. Diese Zellen nutzen Glukose als Energiequelle, und einige (wie Leber und Muskeln) können sie in Form von Kohlenhydraten (Glykogen) speichern. Dieser Mechanismus hilft, den Blutzuckerspiegel auch während des Fastens in einem engen Bereich zu halten, da die Leber kontinuierlich Glukose produziert (über die Glukoneogenese). Die Glukoneogenese wird durch zwei Hormone gesteuert: Insulin (das sie hemmt) und Glukagon (das sie stimuliert). Unter normalen Bedingungen produziert die Leber täglich etwa 250 g Glukose. Die Wirkungen von Insulin lassen sich in zwei Kategorien einteilen:
- Membranwirkungen: Fördert die Aufnahme von Glukose, Aminosäuren und Kalium in Muskel- und Fettzellen.
- Stoffwechselwirkungen: Stimuliert anabole Prozesse (z. B. Glykogen-, Fettsäure- und Proteinsynthese) und ist somit ein „Aufbauhormon”, während es katabole (Abbau-)Prozesse hemmt. Bei Insulinmangel neigen Patienten zu Gewichtsverlust. 2
Positive Wirkungen von Insulin 3:
- Verbessert die kognitiven Funktionen und das Gedächtnis (insbesondere bei intranasaler Verabreichung an Patienten mit Alzheimer oder kognitivem Verfall); schützt die Nervenzellen
- Entspannt die Arterienwände, verbessert die Durchblutung und die Pumpfunktion des Herzens
- Reduziert die Thrombozytenaggregation 4
- Erhöht die Muskelmasse und verbessert die Durchblutung der Muskeln
- Verbessert die Proteinverdauung durch Erhöhung der Pepsinproduktion im Magen 5–6
Die Vorstufe von Insulin ist Proinsulin, das im Verhältnis 1:1 zu Insulin und C-Peptid gespalten wird. Die Messung des C-Peptidspiegels kann zur Beurteilung der Insulinproduktion beitragen. C-Peptid selbst hat ebenfalls wichtige physiologische Wirkungen: Es verbessert die Nierenfunktion, reduziert die Albuminausscheidung, stärkt die Barrierefunktion der Nieren und hilft bei der Wiederherstellung einer normalen Herzfrequenzvariabilität (HRV), wodurch autonome Neuropathien reduziert werden. Darüber hinaus stimuliert es die Natrium-Kalium-ATPase-Aktivität in den Nierentubuli. 7 Zelloberflächenrezeptoren, darunter auch Insulinrezeptoren, funktionieren optimal bei schwankenden Hormonspiegeln – das heißt, sie arbeiten am besten, wenn Insulin intermittierend vorhanden ist. Anhaltig hohe Insulinspiegel können zu einer allmählichen Abnahme der Rezeptorempfindlichkeit und -reaktionsfähigkeit führen, ein Phänomen, das als Insulinresistenz bekannt ist. Dies kann durch zwei Hauptmechanismen geschehen: Internalisierung von Rezeptoren aus der Zelloberfläche und Hemmung intrazellulärer Signalwege. Jedes Gewebe mit Insulinrezeptoren kann insulinresistent werden, aber der Grad der verminderten Insulinsensitivität wird am stärksten von der Leber, den Skelettmuskeln und dem Fettgewebe beeinflusst. 8 Um dem durch die gestörte Glukoseaufnahme verursachten Anstieg des Blutzuckerspiegels entgegenzuwirken, erhöhen die β-Zellen der Bauchspeicheldrüse die Insulinproduktion, was zu einer Hyperinsulinämie führt. Solange die Bauchspeicheldrüse genügend Insulin produziert, um den Blutzuckerspiegel zu regulieren, bleibt dieser im gesunden Bereich. Wenn jedoch die Rezeptorempfindlichkeit weiter abnimmt, kann Glukose nicht mehr effektiv in die Zellen gelangen, was zu einer Hyperglykämie (hoher Blutzucker) führt. Interessanterweise kann Hyperinsulinämie selbst zur Entwicklung einer Insulinresistenz beitragen, sodass unklar ist, was zuerst auftritt. Dies ist klinisch wichtig, da Hyperinsulinämie, insbesondere wenn sie durch eine übermäßige Kalorienaufnahme verursacht wird, ein Auslöser für insulinresistenzbedingte Stoffwechselstörungen sein kann. 9 Insulinresistenz löst eine Kaskade schädlicher Stoffwechselprozesse aus. Zu den unmittelbaren Folgen gehören Hyperglykämie (hoher Blutzucker) und Hypertonie (Bluthochdruck), da die gefäßerweiternde Wirkung des Insulins verloren geht. Dieser Verlust führt zu einer Verhärtung und Verengung der Blutgefäße, was wiederum zu erhöhtem Blutdruck führt. Eine weitere direkte Folge ist Dyslipidämie: erhöhte Triglycerid-, Cholesterin- und LDL-Werte, während das „gute“ Blutfett HDL reduziert ist. In der Folge kommt es häufig zu Hyperurikämie: Hohe Insulinspiegel hemmen die Ausscheidung von Harnsäure über die Nieren. Darüber hinaus ist Insulinresistenz mit chronischen, niedriggradigen Entzündungen verbunden, die durch erhöhte Entzündungsmarker wie CRP gekennzeichnet sind. Insulinresistenz beeinträchtigt auch die Funktion der Endothelzellen, die die Innenfläche der Blutgefäße auskleiden (endotheliale Dysfunktion), und erhöht das Thromboserisiko. Unbehandelt kann Insulinresistenz zu komplexen Erkrankungen wie nichtalkoholischer Fettlebererkrankung (NAFLD), Typ-2-Diabetes und metabolischem Syndrom führen. 10–11 Das metabolische Syndrom – eine Gruppe von Erkrankungen, zu denen erhöhter Blutzucker, abdominale Adipositas, Bluthochdruck und Dyslipidämie gehören – ist in den Industrieländern mittlerweile weit verbreitet und betrifft europäischen Studien zufolge 20–25 % der Bevölkerung. 12

Abbildung 1. Die Folgen der Insulinresistenz
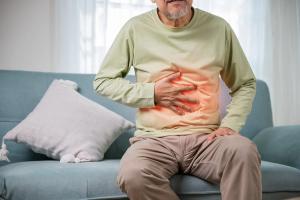
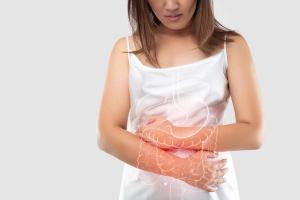
Was sind die Symptome einer Insulinresistenz?
Die Symptome einer Insulinresistenz entwickeln sich in der Regel langsam und schleichend, sodass im Frühstadium kaum Beschwerden auftreten. Mit der Zeit können jedoch verschiedene, oft unspezifische Symptome auftreten, wie Müdigkeit, Tagesmüdigkeit und Konzentrationsschwierigkeiten. Viele Betroffene leiden auch unter Reizbarkeit, Stimmungsschwankungen und erhöhtem Appetit – insbesondere auf Süßes. Bei Frauen kann ein erhöhter Insulinspiegel die Eierstöcke beeinträchtigen, indem er die Produktion von androgene Hormonen (z. B. Testosteron) in den Eierstockzellen anregt. Dies kann zu Menstruationsstörungen und polyzystischem Ovarialsyndrom (PCOS) führen. Aufgrund der Ähnlichkeit von Insulin mit dem insulinähnlichen Wachstumsfaktor 1 (IGF-1), der die Zellvermehrung anregt, können auch sichtbare Hautveränderungen auftreten. Hautzellen können sich schneller teilen, dicker werden und mehr Pigmente produzieren, was zu Acanthosis nigricans führt, einer Erkrankung, die durch dunkle, samtige Flecken in Hautfalten (z. B. am Hals oder in den Achselhöhlen) gekennzeichnet ist. Auch abdominale (viszerale) Adipositas ist häufig, ebenso wie Schwierigkeiten beim Abnehmen, selbst bei gesunder Ernährung und regelmäßiger Bewegung. Diese Ansammlung von Fett in der Bauchhöhle – um die inneren Organe herum – birgt zahlreiche Gesundheitsrisiken. Die Leber spielt dabei eine wichtige Rolle: Sie wandelt überschüssigen Blutzucker in Fett um, um den erhöhten Glukosespiegel zu senken. Dieser Prozess schützt den Körper zwar vor kurzfristigen Schäden durch Hyperglykämie, dient aber auch als evolutionärer Mechanismus zur Energiespeicherung in potenziellen Hungerphasen. Das in der Bauchhöhle gespeicherte Fett wird zu einer leicht zugänglichen Energiereserve. Mit der Zeit trägt dieses viszerale Fett jedoch zu Stoffwechselstörungen, chronischen Entzündungen und Insulinresistenz bei. Menschen, die von IR betroffen sind, verspüren häufig ein verstärktes Hungergefühl, insbesondere nach dem Verzehr kohlenhydratreicher Lebensmittel. Dies ist auf schwankende Blutzuckerwerte zurückzuführen: Eine verminderte Insulinwirksamkeit führt zu schnellen Anstiegen und Abfällen, die wiederum ein stärkeres Verlangen auslösen – insbesondere nach schnell resorbierbaren Kohlenhydraten. 13

Abbildung 2. Die Symptome der Insulinresistenz
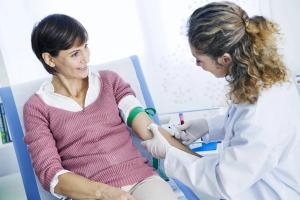
Wie lässt sich Insulinresistenz diagnostizieren?
Insulinresistenz kann lange Zeit symptomfrei bleiben, weshalb eine frühzeitige Erkennung besonders wichtig ist. Verschiedene Labortests können bei der Diagnose helfen, darunter der bereits erwähnte HbA1c-Wert, das C-Peptid (ein Nebenprodukt der Insulinsynthese), der Blutzuckerspiegel und verschiedene aus diesen Werten berechnete Indizes. Die Diagnose beginnt in der Regel mit einer Blutentnahme auf nüchternen Magen, um den Nüchternblutzucker- und Insulinspiegel zu bestimmen. Zusätzlich kann ein oraler Glukosetoleranztest (OGTT) durchgeführt werden. Bei diesem Test trinkt der Patient eine Zuckerlösung und sein Blutzucker- und Insulinspiegel werden in den folgenden Stunden überwacht. Aus diesen Daten lassen sich verschiedene Indizes wie HOMA-IR, QUICKI oder der Matsuda-Index berechnen, um die Insulinsensitivität zu beurteilen. Diese Tests spielen eine wichtige Rolle bei der Früherkennung der Erkrankung, sodass rechtzeitig Lebensstiländerungen oder gegebenenfalls medizinische Maßnahmen ergriffen werden können, um schwerwiegendere Komplikationen zu vermeiden.

Abbildung 3. Methoden zur Messung der Insulinresistenz
Weitere Aspekte bei der Diagnose:
- Körpergewicht und Body-Mass-Index (BMI)
- Hormontests (z. B. Androgene, SHBG, LH/FSH-Verhältnis)
- Gynäkologische Indikatoren (z. B. unregelmäßige Menstruationszyklen, Verdacht auf PCOS)
- Familiäre Vorbelastung (z. B. Typ-2-Diabetes, metabolisches Syndrom) 10
Was sind die Ursachen für Insulinresistenz?
Insulinresistenz kann durch eine Kombination aus genetischer Veranlagung, Umwelteinflüssen und Lebensstilfaktoren wie Bewegungsmangel oder schlechter Ernährung entstehen. Diese Faktoren wirken oft zusammen und tragen gemeinsam zur Entstehung der Erkrankung bei. Während die Genetik bei einigen Menschen eine wichtige Rolle spielen kann, zeigen wissenschaftliche Erkenntnisse, dass in den meisten Fällen erworbene Faktoren wie ein sitzender Lebensstil, ungesunde Ernährungsgewohnheiten, Übergewicht oder Fettleibigkeit und chronischer Stress die Hauptursachen sind.
Bewegungsmangel
Bei körperlicher Aktivität – sei es beim Gehen, Laufen oder anderen Sportarten – steigt der Energiebedarf der Muskeln, die dafür in erster Linie Glukose aus dem Blutkreislauf nutzen. Bemerkenswert ist, dass die Muskeln in diesem Zustand Glukose ohne Insulin aufnehmen können, wodurch der Blutzuckerspiegel auf natürliche Weise sinkt. Regelmäßige Bewegung senkt nicht nur kurzfristig den Blutzuckerspiegel, sondern erhöht mit der Zeit auch die Insulinsensitivität. Bei körperlicher Aktivität setzen die Muskeln biologisch aktive Proteine, sogenannte Myokine (z. B. Irisin), frei, die den Abbau von Fettgewebe unterstützen, Entzündungen hemmen und den Stoffwechsel regulieren. 14 Muskelgewebe dient somit nicht nur der Bewegung, sondern auch als zentraler Regulator des Energiehaushalts und der Blutzuckerkontrolle. Bei intensiver körperlicher Betätigung werden die Muskeln möglicherweise nicht ausreichend mit Sauerstoff versorgt, was zu einem anaeroben Stoffwechsel führt, bei dem Glukose in Milchsäure umgewandelt wird. Dieser Prozess liefert zwar weniger Energie (ATP), ist jedoch schnell und sorgt für eine sofortige Energieversorgung. Später kann die Milchsäure in Gegenwart von Sauerstoff abgebaut oder über den Cori-Zyklus in der Leber wieder in Glukose umgewandelt werden. Dies verhindert die Ansammlung von Milchsäure in den Muskeln und ermöglicht die Wiederverwendung ihrer Energie. Diese Umwandlung von Glukose erfordert jedoch zusätzliche Energie, die der Körper aus dem Fettabbau (Beta-Oxidation) gewinnt und so effektiv in einen Zustand der Fettverbrennung wechselt. Interessanterweise hemmt der Körper vorübergehend die Verwendung von Glukose, wenn die Leber Glukose produziert, um gleichzeitige „entgegengesetzte” Prozesse zu vermeiden. Nach dem Training nehmen die erschöpften Muskeln wieder Glukose auf und speichern sie, wodurch Blutzuckerspitzen und -tiefs ausgeglichen werden. Ohne regelmäßige körperliche Aktivität bricht diese metabolische Synergie zusammen: Die Leber produziert weiterhin zu viel Glukose, während die Muskeln nicht an der Zuckerverwertung beteiligt sind. Diese „metabolische Schuld” kann sich mit der Zeit verschlimmern. Bewegung unterstützt die Energieverwertung, verbessert die Insulinsensitivität, gleicht den Blutzucker aus und entlastet die Leber. Darüber hinaus hilft die Muskelmasse, den Stoffwechsel auch in Ruhe aufrechtzuerhalten. 15
Die Rolle von Adipositas bei der Entstehung von Insulinresistenz
Adipositas, insbesondere die Ansammlung von abdominalen (viszeralem) Fett, spielt eine zentrale Rolle bei der Entstehung von Insulinresistenz. Fettgewebe ist nicht nur eine Energiereserve, sondern fungiert auch als endokrines Organ, das Adipokine, inflammatorische Zytokine (z. B. TNF-α, IL-6) und freie Fettsäuren (FFAs) ausschüttet. 16 Diese Substanzen stören die Signalwege des Insulins in den Zellen und verringern die Glukoseaufnahme – insbesondere in Muskel- und Fettgewebe. Die mit Adipositas einhergehende chronische, niedriggradige Entzündung verstärkt diesen Effekt und trägt direkt zur Aufrechterhaltung der Insulinresistenz bei. Insbesondere viszerales Fett produziert höhere Mengen an Entzündungsmediatoren, die die Insulinwirkung stärker beeinträchtigen als andere Fettarten. Es ist wichtig zu beachten, dass nicht alles Fettgewebe gleich ist. Viszerales Fett (Fett um die inneren Organe) produziert viel mehr Hormone und hat einen stärkeren Einfluss auf die Insulinresistenz, während subkutanes Fett (direkt unter der Haut) eine moderatere Wirkung hat. Dieser Unterschied erklärt, warum Apfel-Fettverteilung (zentrale oder abdominale Fettverteilung) enger mit Insulinresistenz und metabolischem Syndrom verbunden ist als Birnen-Fettverteilung (Fett um die Hüften), die überwiegend subkutan ist. 17–18
Verzehr von Lebensmitteln mit hohem glykämischen Index
Fettleibigkeit wird oft als Folge einer übermäßigen Kalorienaufnahme angesehen, aber es ist wichtig zu verstehen, dass übermäßiges Essen allein schwerwiegende physiologische Folgen haben kann. Selbst eine kurzfristige Ernährung mit hohem Energiegehalt kann die Insulinempfindlichkeit des Gehirns verringern, unabhängig von einem Rückgang der Insulinempfindlichkeit in den peripheren Geweben. Eine übermäßige Kalorienaufnahme beeinträchtigt die Signalwege des Insulins in den Gehirnzellen, verändert das Darmmikrobiom, aktiviert Signalwege der Entzündung und stört letztlich die Gehirnfunktion. Dadurch entsteht ein Teufelskreis, in dem molekulare Veränderungen im Gehirn Neuroinflammation auslösen und im Laufe der Zeit zu Erkrankungen wie Depressionen, kognitivem Verfall, Alzheimer und anderen neurologischen Störungen beitragen. Weitere Risikofaktoren sind Darmdysbiose (unausgewogene Mikrobiota), die Freisetzung von Endotoxinen aus Bakterien und eine erhöhte Darmpermeabilität. Entzündungen, die im Fettgewebe beginnen, können sich auf das Gehirn ausbreiten und die Insulinsensitivität im zentralen Nervensystem weiter verringern. 19 Der Fettstoffwechsel gewinnt im Zusammenhang mit Adipositas zunehmend an Bedeutung. Wenn das Blut überschüssige Fettsäuren enthält, schalten die Zellen auf Fettverbrennung um, um Energie zu gewinnen, wodurch der Kohlenhydratstoffwechsel unterdrückt wird – ein Prozess, der für einen stabilen Blutzuckerspiegel, niedrigen Insulinspiegel und eine effiziente Energienutzung. Diese kompetitive, sich gegenseitig hemmende Beziehung zwischen Fett- und Kohlenhydratstoffwechsel wird durch den Randle-Zyklus beschrieben. Bei übergewichtigen Personen führen erhöhte FFA zu einem Energieüberschuss auf zellulärer Ebene, wodurch die Glukoseaufnahme reduziert wird und direkt zu Insulinresistenz und Typ-2-Diabetes beiträgt. Interessanterweise kann eine Kalorienrestriktion allein – unabhängig von der Kohlenhydrataufnahme – den Blutzucker- und Insulinspiegel senken. 20
Chronische Entzündungen
Adipositas führt zu anhaltenden, leichten systemischen Entzündungen, die eine wichtige Rolle bei der Entwicklung von Langzeitkomplikationen im Zusammenhang mit Typ-2-Diabetes spielen – wie nichtalkoholische Fettlebererkrankungen, Retinopathie, Herz-Kreislauf-Erkrankungen und Nierenschäden (Nephropathie). Diese Entzündung hilft auch, den Zusammenhang zwischen Diabetes und anderen Erkrankungen wie Alzheimer, polyzystischem Ovarialsyndrom (PCOS), Gicht und rheumatoider Arthritis zu erklären. Chronische Entzündungen betreffen insbesondere insulinempfindliche Gewebe wie Fettgewebe, Leber, Muskeln und Bauchspeicheldrüse. Dieses als Immunometabolismus bezeichnete Phänomen bezeichnet die enge, wechselseitige Beziehung zwischen dem Immunsystem und dem Stoffwechsel. Stoffwechselstörungen lösen Entzündungsreaktionen aus, die wiederum den Stoffwechsel weiter stören. Mit zunehmender Fettmasse und abnehmender Insulinsensitivität steigt die Produktion von proinflammatorischen Zytokinen, während der Spiegel von Adiponektin – einem für den Stoffwechsel nützlichen Hormon – sinkt. Dieses Ungleichgewicht verändert auch die Zusammensetzung der Immunzellen im Fettgewebe, wodurch proinflammatorische M1-Makrophagen zunehmen und antiinflammatorische M2-Makrophagen abnehmen 21. Die Ansammlung und Aktivierung von Makrophagen sind die Hauptursachen für chronische Entzündungen im stoffwechselaktive Gewebe, aber auch andere Immunzellen – wie T- und B-Lymphozyten – tragen zu diesem entzündlichen Milieu bei. 22
Stress, Schlafmangel
Stress trägt nachweislich erheblich zur Entstehung von Typ-2-Diabetes bei. Er entsteht, wenn der Körper auf einen Reiz trifft, dem er widerstehen oder an den er sich anpassen muss, und löst die Mobilisierung von Energie aus. Diese Reize können physischer (z. B. Temperatur, Strahlung), chemischer oder biologischer (z. B. Infektionen) oder psychologischer Natur sein. Während kurzfristiger Stress eine notwendige und vorteilhafte Reaktion ist, die das Überleben fördert, entstehen Probleme, wenn Stress intensiv, lang anhaltend oder chronisch ist, da dies die Anpassung Ressourcen des Körpers erschöpfen kann. Während der klassischen „Kampf-oder-Flucht”-Reaktion schaltet der Körper auf katabolen Stoffwechsel um, um schnell Energie zu mobilisieren, während weniger unmittelbare Prozesse wie Verdauung, Wachstum, Fortpflanzung und Immunfunktion unterdrückt werden. Diese evolutionäre Reaktion, die ursprünglich dazu diente, Menschen bei der Flucht vor Raubtieren zu helfen, wird durch die schnelle Mobilisierung sofort verfügbarer Energiereserven (z. B. Glukose) angetrieben. 23 In solchen Fällen produziert der Körper Stresshormone, vor allem Glukokortikoide (z. B. Cortisol) und Katecholamine (z. B. Adrenalin). Diese Hormone regen die Leber zur verstärkten Glukoneogenese an, wodurch der Blutzuckerspiegel ansteigt, um eine schnelle Energiequelle bereitzustellen. Wenn dieser Glukoseanstieg jedoch nicht wie in der modernen Lebensweise häufig der Fall ist, nicht durch körperliche Aktivität gefolgt wird, bleibt der Blutzuckerspiegel erhöht, was schließlich zu einer chronischen Hyperglykämie beiträgt. Mit der Zeit fördert dies die Insulinresistenz. Cortisol hemmt auch die Glukoseaufnahme durch die Muskelzellen und verringert so deren Beitrag zur Blutzuckerregulation. In der heutigen Welt geht chronischer Stress häufig mit Bewegungsmangel, unregelmäßigen Essgewohnheiten oder einer ungesunden Ernährung einher – Faktoren, die den Stoffwechsel weiter stören und zur Entwicklung von viszeraler (abdominaler) Adipositas beitragen. 23 Nicht nur Stress, sondern auch die Quantität und Qualität des Schlafs haben einen erheblichen Einfluss auf die Insulinsensitivität. Der moderne Lebensstil – geprägt von langen Arbeitszeiten, Leistungsdruck in der Schule und übermäßiger Bildschirmnutzung – führt häufig zu Schlafmangel 24. Obwohl die genauen kausalen Mechanismen noch nicht vollständig geklärt sind, erhöht unzureichender Schlaf Entzündungen und kann zu Insulinresistenz und Typ-2-Diabetes beitragen, selbst wenn keine Gewichtszunahme vorliegt. 25 Experten empfehlen Erwachsenen mindestens sieben Stunden Schlaf pro Nacht, um einen gesunden Stoffwechsel aufrechtzuerhalten. 26
Die Rolle des Darmmikrobiota
Menschen mit Insulinresistenz weisen häufig ein Ungleichgewicht in ihrer Darmflora auf, das als Dysbiose bezeichnet wird und eine ursächliche Rolle bei der Störung des Glukosestoffwechsels und der Persistenz chronischer Low-Grade-Entzündungen spielt. Eine abnormale Aktivität des Darmmikrobiota erhöht die Durchlässigkeit des Darms, sodass Bakterien und Lipopolysaccharide (LPS) – entzündungsfördernde Bestandteile der Bakterienzellwände – in den Blutkreislauf gelangen können. Dieser als metabolische Endotoxämie bezeichnete Zustand trägt zu systemischen Entzündungen bei, die ein wichtiger Faktor für die Entwicklung von Insulinresistenz, metabolischem Syndrom und sogar bestimmten Krebsarten sind.
Eine Dysbiose kann entweder mit einer Abnahme nützlicher Bakterien (z. B. Akkermansia muciniphila, Faecalibacterium prausnitzii) und/oder einer übermäßigen Vermehrung proinflammatorischer Stämme (z. B. bestimmte Proteobacteria- oder Firmicutes-Arten) einhergehen. Eine verminderte Produktion von kurzkettigen Fettsäuren (SCFAs) – insbesondere Butyrat – durch diese nützlichen Mikroben schwächt die Darmbarriere und verschlimmert systemische Entzündungen.
Über Entzündungen hinaus kann das Darmmikrobiom auch direkt die Insulinwirkung beeinflussen. Einige Bakterienstämme erhöhen die Insulinsensitivität und verbessern den Glukosestoffwechsel. In Versuchsmodellen senkte die Einführung dieser Stämme in den Darm den Blutzuckerspiegel, reduzierte den Gehalt an Einfachzuckern im Stuhl, verbesserte das Lipidprofil und linderte die Symptome der Insulinresistenz. Umgekehrt fördert überschüssiger Zucker, der im Darm unverarbeitet verbleibt, die Fettspeicherung und Entzündungen und erhöht das Risiko für Fettleibigkeit. 27
Die Darmflora von insulinresistenten Personen unterscheidet sich deutlich von derjenigen insulinempfindlicher Personen. Bei ersteren dominieren Bakterien der Gattungen Blautia und Dorea (Familie Lachnospiraceae), während bei letzteren Alistipes- und Bacteroides-Arten häufiger vorkommen. Letztere Arten verstoffwechseln Kohlenhydrate effizienter, sodass weniger Zucker im Darm verbleibt. Die orale Verabreichung von Alistipes indistinctus schützt sogar vor Fettleibigkeit und Insulinresistenz, selbst wenn die Probanden eine fettreiche Ernährung zu sich nehmen 8. Mehrere Studien haben Zusammenhänge zwischen der Zusammensetzung der Darmmikrobiota, Plasmametabolite (z. B. verzweigtkettige Aminosäuren (BCAAs), SCFAs und LPS), verschiedenen Formen der Adipositas und bestimmten Diabetes-Typen (z. B. insulinresistent vs. insulinmangelhaft) sowie Umwelteinflüssen. Bei Adipositas nehmen die Populationen von Faecalibacterium prausnitzii, Akkermansia, Oscillibacter und Intestinimonas tendenziell ab, während bei Typ-2-Diabetes Escherichia/Shigella-Stämme häufig zunehmen. 1
Kurzkettige Fettsäuren (SCFAs) – insbesondere Acetat, Propionat und Butyrat –, die von Darmbakterien produziert werden, spielen eine entscheidende Rolle bei der Regulierung des Stoffwechsels, des Appetits und der Insulinsensitivität. Ihre Konzentrationen und Verhältnisse im Stuhl oder Plasmacan dienen als nützliche Biomarker zur Beurteilung des Schweregrads der Insulinresistenz. Butyrat und Propionat haben in der Regel eine antiadipöse Wirkung: Sie fördern Leptin und andere Sättigungshormone, reduzieren Entzündungen und verbessern die Insulinsensitivität. Propionat trägt als Substrat der Glukoneogenese zur Stabilisierung des Blutzuckerspiegels bei, kann jedoch in Überschuss die Insulinresistenz fördern, indem es die Insulin- und Glukagonsekretion stimuliert und das sympathische Nervensystem aktiviert 28. Acetat stimuliert Ghrelin (das Hungerhormon) und fördert so den Appetit, die Fettspeicherung und eine mögliche Gewichtszunahme 29. Ein Rückgang der Butyrat produzierenden Bakterien – wie Faecalibacterium prausnitzii und Roseburia intestinalis – ist ein Kennzeichen für Insulinresistenz. Ihr Fehlen trägt zu erhöhten Entzündungen und einer verminderten Stoffwechselfunktion des Darms bei. 30
Ein höherer Gehalt an Akkermansia muciniphila und Parabacteroides distasonis im Darm steht in Zusammenhang mit einer verbesserten Insulinsensitivität bei Kalorienrestriktion, was die schützende Rolle dieser Spezies unterstreicht. 30
Die Untersuchung der Zusammensetzung und Funktion des Darmmikrobiota könnte zu einem wertvollen Instrument für die Diagnose und Behandlung von Insulinresistenz werden.
Darm-Hirn-Achse
Die Darm-Hirn-Achse ist ein bidirektionaler Kommunikationsweg, über den die Darmmikrobiota, das Nervensystem, das endokrine System und das Immunsystem interagieren. Dieses komplexe Netzwerk spielt eine besonders wichtige Rolle bei der Regulierung des Stoffwechsels. Die Darmmikrobiota trägt nicht nur zur Verdauung bei, sondern beeinflusst auch die Gehirnfunktion über neuronale, hormonelle und immunologische Mechanismen. Eine nährstoffreiche, aber unausgewogene Ernährung sowie Fettleibigkeit können die Zusammensetzung des Darmmikrobiota verändern. Die von diesen Mikroben produzierten Metaboliten können Signale an das Gehirn senden, häufig über den Vagusnerv. Enteroendokrine Zellen, die sich in der Darmschleimhaut befinden, fungieren sowohl als Sensoren als auch als Hormon-Produzenten. Sie erkennen Veränderungen in der Darmmilieu – wie Nährstoffe oder mikrobielle Aktivität – und scheiden verschiedene Darmhormone wie GLP-1, PYY und CCK aus. Diese Hormone beeinflussen nicht nur die Insulinausschüttung und den Blutzuckerspiegel, sondern auch den Appetit, die Stimmung und sogar Lern- und Gedächtnisprozesse. Das Immunsystem spielt ebenfalls eine wichtige Rolle in der Darm-Hirn-Achse. Aktivierte Immunzellen – wie Th1-, Th17-, Treg-Zellen, Neutrophile und Makrophagen – können Entzündungssignale aussenden, die die Gehirnfunktion beeinträchtigen und das Gleichgewicht zwischen Darm und Gehirn stören. Wenn die Darmbarriere geschwächt ist, können schädliche Substanzen in den Blutkreislauf gelangen – dies wird als „Leaky Gut“ (durchlässiger Darm) bezeichnet. Dieser Zustand verstärkt systemische Entzündungen, die nicht nur die Gehirnfunktion beeinträchtigen, sondern auch die Insulinresistenz verschlimmern. 19

Abbildung 4. Mögliche Ursachen der Insulinresistenz
Mitochondriale Funktion
Bei Insulinresistenz nimmt die Energieverwertung der Zellen aufgrund mehrerer Faktoren ab: einer Verringerung der Anzahl der Mitochondrien und ihrer oxidativen Enzyme, einer beeinträchtigten ATP-Produktion und strukturellen Veränderungen in den Mitochondrien. ATP (Adenosintriphosphat) ist der wichtigste Energieträger des Körpers, und jeden Tag verbrauchen wir eine Menge, die unserem gesamten Körpergewicht entspricht. Diese Energie muss kontinuierlich durch die Mitochondrien regeneriert werden. Eine übermäßige Kalorienaufnahme erhöht die Produktion reaktiver Sauerstoffspezies (ROS), die die Mitochondrien schädigen, Entzündungen auslösen und Immunzellen im Nervensystem aktivieren. Die Ansammlung von Fett in den Zellen verringert ebenfalls die oxidative Kapazität, insbesondere bei Personen mit einer genetischen Veranlagung. 31 Mitochondrien können nicht nur durch verschiedene Stoffwechselstörungen geschädigt werden, sondern auch durch den Alterungsprozess, der ihre Leistungsfähigkeit allmählich beeinträchtigt. Mit der Zeit sinkt der Spiegel wichtiger Hormone wie Wachstumshormon und IGF-1, die beide diese energieproduzierenden Organellen unterstützen, wodurch das Risiko für Stoffwechselerkrankungen steigt. 32 Eine optimale Mitochondrienfunktion ist für eine ausreichende Insulinreaktion unerlässlich. Etwa 3 % der Menschen mit Diabetes leiden an mitochondrialem Diabetes (MIDD), der entweder Typ-1- oder Typ-2-Diabetes ähneln kann. Die Erkrankung ist durch eine β-Zell-Dysfunktion und eine verminderte Insulinsensitivität im Muskelgewebe gekennzeichnet, die sich beide mit zunehmendem Alter verschlimmern. 33–34 Innerhalb der Zellen benötigen Mitochondrien auch Wasser, um richtig zu funktionieren – und es ist vorteilhaft, wenn dieses Wasser einen geringen Deuteriumgehalt aufweist. Deuterium ist ein schweres Isotop des Wasserstoffs, das zusätzlich zum Proton ein Neutron enthält. Es kommt natürlicherweise in Trinkwasser in einer Konzentration von etwa 150 ppm vor, wobei dies geografisch variiert (in höheren Lagen und im Landesinneren sind die Werte niedriger). 35 Der letzte Schritt der zellulären Energieproduktion findet in der Elektronentransportkette (oder Redoxkette) innerhalb der inneren Mitochondrienmembran statt, die aus fünf Komplexen besteht. Der Komplex V wirkt wie eine mikroskopische Turbine und leitet Protonen, die von den vier vorherigen Komplexen in den Intermembranraum gepumpt wurden, zurück in die Mitochondrienmatrix, um die ATP-Synthese anzutreiben. Wenn Deuterium den Komplex V passiert, kann es den Mechanismus beschädigen und die Fähigkeit der Mitochondrien zur Energieproduktion verringern. Aus metabolischer Sicht sind Fette ein besserer Brennstoff als Kohlenhydrate, da sie mehr Wasserstoff und weniger Deuterium enthalten. Infolgedessen entsteht bei der Fettoxidation Stoffwechselwasser, das von Natur aus weniger Deuterium enthält als Trinkwasser. Erhöhte Deuteriumwerte in den Zellen beeinträchtigen die Energieproduktion der Mitochondrien, verstärken Entzündungen und können die Insulinsensitivität verringern. Die Darmmikrobiota spielt hier ebenfalls eine schützende Rolle, indem sie Wasserstoffgas und kurzkettige Fettsäuren (z. B. Buttersäure, Butyrat, Acetat) produziert, die alle die Gesundheit der Mitochondrien und den Stoffwechsel unterstützen. Bemerkenswert ist, dass der im Darm erzeugte Wasserstoffgas arm an Deuterium ist und somit die Energieproduktion der Zellen schützt. Insbesondere Buttersäure dient als wichtige Energiequelle für Kolonozyten (Zellen des Dickdarms), reguliert Entzündungen und unterstützt eine gesunde Zellfunktion. Auf diese Weise trägt das Darmmikrobiom indirekt und direkt zu einem optimalen Energiestoffwechsel bei. 36
Was sind die Folgen einer Insulinresistenz?
Anhaltend erhöhte Blutzuckerwerte infolge einer Insulinresistenz können zu schwerwiegenden Langzeitkomplikationen führen, insbesondere im Gefäßsystem. Die frühesten Schäden treten oft in den kleinsten Blutgefäßen auf – dies wird als mikrovaskuläre Schädigung bezeichnet. Diese Veränderungen betreffen mehrere lebenswichtige Organe:
- Augen: Schäden am feinen Netz der Blutgefäße in der Netzhaut können zu einer diabetischen Retinopathie führen, die zu Sehverlust oder sogar zur Erblindung führen kann.
- Nieren: Schäden an den kleinen Blutgefäßen der Nieren können eine diabetische Nephropathie verursachen, die zu Nierenversagen führen und eine Dialyse erforderlich machen kann.
- Nervensystem: Eine beeinträchtigte Blutversorgung kleiner Nerven kann zu einer peripheren Neuropathie führen, die sensorische Störungen, Taubheitsgefühle, Schmerzen oder Muskelschwäche, insbesondere in den Händen und Füßen, zur Folge hat.
Diese Veränderungen betreffen jedoch nicht nur die peripheren Körperteile, sondern auch das zentrale Nervensystem – insbesondere das Gehirn. Schädigungen der kleinen Blutgefäße im Gehirn können zu Demenz (kognitiver Verfall), Schlaganfall, Stimmungsstörungen wie Depressionen und Angstzuständen sowie Gleichgewichtsstörungen und Gangunsicherheit beitragen. Ebenso können Schädigungen der kleinen Blutgefäße des Herzmuskels zu Brustschmerzen (Angina pectoris) führen und zu einer strukturellen und funktionellen Verschlechterung des Herzens (Kardiomyopathie) beitragen. Schädigungen der größeren Blutgefäße werden als makrovaskuläre Komplikationen bezeichnet und umfassen häufig:
- Periphere arterielle Verschlusskrankheit (PAVK): Verengung oder Verstopfung der Arterien in den Gliedmaßen – meist in den Beinen – was zu Schmerzen beim Gehen, kalten Extremitäten, verzögerter Wundheilung und in schweren Fällen zu Geschwüren oder Amputationen führt.
- Koronare Herzkrankheit (KHK): Eine Verstopfung oder Verengung der Herzarterien, die den Herzmuskel versorgen, kann zu Angina pectoris, Herzinfarkten oder Herzinsuffizienz führen.
- Schlaganfall: Plötzlicher Ausfall der Blutversorgung des Gehirns. Es gibt zwei Haupttypen:
- Ischämischer Schlaganfall: Verursacht durch eine verstopfte Arterie (z. B. durch ein Blutgerinnsel)
- Hämorrhagischer Schlaganfall: Verursacht durch ein gerissenes Blutgefäß, das zu einer Blutung im Gehirn führt
Beide Arten von Schlaganfällen können schwerwiegende Folgen haben, darunter Lähmungen, Sprachstörungen, Gedächtnisverlust oder Tod. Eine schnell zunehmende Erkrankung, die eng mit Insulinresistenz verbunden ist, ist die nichtalkoholische Fettlebererkrankung (NAFLD). Bei dieser Erkrankung sammelt sich Fett in der Leber an, obwohl kein Alkohol konsumiert wird. Mit der Zeit kann diese Fettansammlung zu Entzündungen, Zellschäden und Fibrose (Vernarbung) führen, wodurch die Leberfunktion beeinträchtigt wird und sich möglicherweise eine Leberzirrhose entwickelt. NAFLD tritt sehr häufig bei Menschen mit Insulinresistenz und Typ-2-Diabetes auf. Alarmierend ist, dass die Prävalenz weltweit steigt – auch bei Kindern. Daher sollten alle medizinischen Fachkräfte, die Patienten mit Insulinresistenz behandeln – ob Allgemeinmediziner, Ernährungsberater oder Internisten – die Früherkennung und Behandlung von Fettleber auch ohne Symptome priorisieren. 10
Welche Behandlungsmöglichkeiten gibt es für Insulinresistenz?
Konventionelle Medizin
Die meisten Medikamente, die derzeit in der klinischen Praxis zur Behandlung des Kohlenhydratstoffwechsels eingesetzt werden, konzentrieren sich in erster Linie auf die Regulierung des Blutzuckerspiegels. Diese Medikamente wurden nicht speziell zur Behandlung der mit Insulinresistenz verbundenen Komplikationen wie Retinopathie, nichtalkoholische Fettlebererkrankung oder chronische Entzündungen entwickelt. Einige haben zwar sekundäre Vorteile für diese Erkrankungen, aber nur eines – Metformin – hat eine Fähigkeit zur Verlangsamung des Krankheitsverlaufs gezeigt. 22 Metformin ist das Medikament der ersten Wahl zur Behandlung von Insulinresistenz, insbesondere bei Prädiabetes und Typ-2-Diabetes. Es reduziert in erster Linie die Glukoseproduktion in der Leber und erhöht außerdem die Insulinsensitivität in peripheren Geweben. Es verursacht keine Hypoglykämie und ist aufgrund seiner gewichtsreduzierenden Wirkung besonders für übergewichtige oder adipöse Patienten geeignet. Laut der Diabetes Prevention Program (DPP)-Studie senkte Metformin das Risiko, an Typ-2-Diabetes zu erkranken, bei insulinresistenten Personen um etwa 30 %. Die Behandlung wird im Allgemeinen gut vertragen, obwohl anfangs gastrointestinale Nebenwirkungen wie Blähungen oder Durchfall auftreten können. 37 Metformin beeinflusst auch das Darmmikrobiom. Im Vergleich zu unbehandelten Typ-2-Diabetes-Patienten zeigen Patienten, die Metformin einnehmen, eine erhöhte Häufigkeit von Parabacteroides distasonis, eine verbesserte Integrität der tight junctions in den Darmepithelzellen und eine Zusammensetzung des Mikrobioms, die der von gesunden Personen ähnlicher ist. Interessanterweise können bestimmte Darmmikrobiom-Profile die Reaktion eines Patienten auf Metformin oder dessen Nebenwirkungen vorhersagen. Eine höhere Präsenz von Segatella copri (früher Prevotella copri) ist mit einer geringeren Wirksamkeit bei der Senkung des HbA1c-Wertes verbunden. Der HbA1c-Wert spiegelt den durchschnittlichen Blutzuckerspiegel der letzten 2–3 Monate wider. Im Gegensatz dazu kann eine höhere Präsenz von Streptococcus parasanguinis auf ein höheres Risiko für Nebenwirkungen hinweisen. Da diese mikrobiellen Muster auch durch gleichzeitig eingenommene Medikamente (z. B. Protonenpumpenhemmer, Antikoagulanzien) beeinflusst werden können, kann die Analyse des Darmmikrobiota entscheidend sein, um zu verstehen, wie sich eine Polypharmazie auf die Wirksamkeit von Metformin auswirkt. 30
Gewichtsabnahme: Empfehlungen zu Ernährung und Bewegung
Eine kohlenhydratarme Ernährung kann vorübergehend die Insulinsensitivität verbessern, insbesondere bei erhöhten Blutzucker- und Blutfettwerten. Eine Reduzierung der Kohlenhydratzufuhr kann die Fettverbrennung unterstützen und die Stoffwechselüberlastung verringern. Allerdings können traditionelle kohlenhydratarme oder ketogene Diäten aufgrund ihres hohen Fettgehalts den Kohlenhydratstoffwechsel mit der Zeit beeinträchtigen und möglicherweise zu einer physiologischen Insulinresistenz führen. In diesem Zustand verlieren die Zellen die Fähigkeit, Kohlenhydrate effizient zu verarbeiten. Der Schlüssel zu einem stabilen Stoffwechsel ist die metabolische Flexibilität – die Fähigkeit des Körpers, zwischen Fett und Kohlenhydraten als Energiequellen zu wechseln. Die Wiederherstellung eines gesunden Kohlenhydratstoffwechsels ist daher unerlässlich. Das Ziel sollte nicht eine dauerhafte Kohlenhydratrestriktion sein, sondern die schrittweise und intelligente Wiedereinführung von Kohlenhydraten, damit der Körper wieder lernt, diese effektiv zu verwerten. 20 Richtig ausgewählte körperliche Aktivität unterstützt diesen Prozess ebenfalls, indem sie die Insulinsensitivität der Skelettmuskulatur erhöht und das Darmmikrobiom positiv beeinflusst. Während sehr intensives Training das Verdauungssystem belasten und möglicherweise zu Dysbiose oder einem trainingsinduzierten gastrointestinalen Syndrom führen kann, hat moderate körperliche Aktivität positive Auswirkungen. Sie erhöht den Anteil von Bakterien wie Akkermansia muciniphila und Oscillospira und fördert die Produktion von kurzkettigen Fettsäuren (SCFAs) sowie Milchsäure. Diese Verbindungen sind nicht nur für die Darmgesundheit wichtig, sondern verbessern auch indirekt die Stoffwechselflexibilität und Insulinsensitivität. 30
Funktionsmedizin
Die Wiederherstellung der Darmgesundheit ist ein wichtiger Schritt zur Verbesserung der Stoffwechselfunktion und steht im Mittelpunkt der funktionelle medizinische Ansätze. Die Grundlage bilden eine personalisierte Ernährung, Anpassungen des Lebensstils und pflanzliche, natürliche Therapien, die auf die individuellen Bedürfnisse zugeschnitten sind.
Gezielte Nahrungsergänzung und Nährstoffersatz
Eine Vielzahl natürlicher Verbindungen und Mikronährstoffe kann die Behandlung der Insulinresistenz unterstützen, indem sie Entzündungen hemmen, oxidativen Stress reduzieren und die Insulinwirkung verbessern. Berberin, Quercetin und Omega-3-Fettsäuren, die starke entzündungshemmende Eigenschaften haben und zur Wiederherstellung der Insulinsensitivität beitragen können. Antioxidantien wie Vitamin C und E, Selen und Resveratrol, die oxidative Schäden bekämpfen – ein Schlüsselfaktor für die Entstehung und das Fortschreiten der Insulinresistenz. Vitamin D, das den Kalzium- und Phosphorstoffwechsel unterstützt und auch proinflammatorische Zytokine reduziert. Studien haben gezeigt, dass Vitamin D die Insulinrezeptordichte in Muskeln, Leber und Fettgewebe erhöht und so sowohl die Insulinsensitivität als auch die Glukoseverwertung verbessert. 38 Inositol (insbesondere in den Formen Myo-Inositol und D-Chiro-Inositol) ist ein vielversprechendes Nahrungsergänzungsmittel bei Insulinresistenz. Es verbessert die Insulinsignalisierung, senkt den Nüchtern-Insulinspiegel und hilft bei der Regulierung des Menstruationszyklus bei Frauen mit PCOS, die häufig unter Insulinresistenz leiden. 39 Chrom ist ein essentielles Spurenelement, das die Insulinfunktion und den Stoffwechsel von Kohlenhydraten, Fetten und Proteinen unterstützt. Eine Supplementierung kann den Nüchternblutzucker verbessern und die Insulinresistenz verringern. 40 Zimt verbessert die Insulinrezeptor-Funktion, fördert die Glukoseaufnahme und hemmt die Glukoseproduktion in der Leber. Seine antioxidativen und entzündungshemmenden Wirkungen tragen zur Normalisierung des Blutzuckers, der Lipidwerte und des Blutdrucks bei und helfen so, Typ-2-Diabetes vorzubeugen. 41 Selen schützt die Zellen vor oxidativen Schäden, die die Insulinfunktion beeinträchtigen können, während Zink eine entscheidende Rolle bei der Insulinsynthese, -speicherung und -sekretion spielt und so indirekt den Glukosestoffwechsel verbessert. 42–43 Kombinationen dieser Nährstoffe sind oft wirksamer als einzelne Verbindungen, da sie synergistisch wirken, um Entzündungen zu reduzieren, oxidativen Stress zu senken, die Insulinsensitivität zu verbessern und die Wiederherstellung des Stoffwechsels zu unterstützen.
Ernährungsrichtlinien
Eine glykämisch niedrige Ernährung ist eine der grundlegenden Strategien zur Wiederherstellung der Stoffwechselgesundheit. Es ist ratsam, häufig ausgewogene Mahlzeiten zu sich zu nehmen, die eine Kombination aus Proteinen, gesunden Fetten und komplexen Kohlenhydraten enthalten, auch nachmittags und abends. Fasten sollte mit Vorsicht angegangen werden – insbesondere zu Beginn der Behandlung –, da ein plötzlicher Abfall des Blutzuckerspiegels den Körper belasten kann. Sobald sich der Energiestoffwechsel stabilisiert hat, können die Mahlzeiten-Intervalle schrittweise verlängert werden. Die Unterstützung der Mitochondrienfunktion kann ebenfalls von entscheidender Bedeutung sein, insbesondere bei Menschen mit Diabetes oder bei Einnahme von Metformin. Denn Metformin hemmt teilweise den Komplex I in der mitochondrialen Atmungskette. Langfristig kann dies zu Problemen bei der Energieproduktion, Vitamin-B12-Mangel und in seltenen Fällen zu einer Laktatazidose führen. Daher wird häufig die Einnahme von Nahrungsergänzungsmitteln empfohlen, die die Gesundheit der Mitochondrien unterstützen, wie z. B.: Vitamin B12 (Methylcobalamin), Alpha-Liponsäure, Coenzym Q10 (CoQ10), Vitamin B1 (Benfotiamin), Taurin, Magnesium und andere mitochondriale Cofaktoren. 44 Weitere vorteilhafte Ernährungsansätze sind die mediterrane Ernährung, die reich an Gemüse, gesunden Fetten (z. B. Olivenöl) und moderaten Mengen Fisch ist, sowie moderates, zeitlich gut abgestimmtes intermittierendes Fasten, das zur Wiederherstellung der metabolischen Flexibilität beitragen kann.
Die Rolle von Präbiotika und Probiotika
Probiotika – insbesondere bestimmte Stämme von Lactobacillus und Bifidobacterium – verbessern nachweislich das Blutfettprofil und senken den Nüchternblutzucker, den Insulinspiegel und HbA1c. Ein besonders vielversprechender Stamm, Akkermansia muciniphila, stärkt nachweislich die Darmbarriere, wirkt entzündungshemmend und verbessert die Stoffwechselfunktion. Die kombinierte Verwendung von Präbiotika und Probiotika (bekannt als Synbiotika) hat zusätzliche Vorteile bei der Senkung von Hyperglykämie und der Unterstützung der Gewichtsabnahme gezeigt. Individuelle Unterschiede in der Zusammensetzung der Darmmikrobiota können ebenfalls die Wirksamkeit von Ernährungs- und Nahrungsergänzungsmittel beeinflussen. Beispielsweise sprechen Menschen mit einer von Bacteroides dominierten Darmflora tendenziell gut auf Capsaicin an, einen natürlichen Wirkstoff, der auch als Präbiotikum wirkt. Bei Personen mit einem hohen Prevotella:Bacteroides-Verhältnis hat Arabinoxylan – eine Art präbiotische Hemicellulose – eine schützende Wirkung gegen Gewichtszunahme gezeigt. 30
Lebensstil
Regelmäßige Bewegung, effektives Stressmanagement und eine gute Schlafqualität haben einen erheblichen Einfluss sowohl auf die Zusammensetzung der Darmmikrobiota als auch auf die allgemeine Stoffwechselgesundheit. Diese Lebensstilfaktoren können eine hochwirksame Rolle bei der umfassenden Behandlung von Insulinresistenz spielen – nicht nur allein, sondern auch in Synergie mit den oben genannten Ernährungs- und Nahrungsergänzung Strategien.
Fragen Sie unsere Experten!
Insulinresistenz ist eine komplexe Stoffwechselstörung, die mehrere Organsysteme betrifft. Eine wirksame Behandlung erfordert einen integrierten, mehrschichtigen Ansatz. Wir bei HealWays glauben, dass eine symptomorientierte Behandlung nicht ausreicht. Um echte, dauerhafte Ergebnisse zu erzielen, ist es unerlässlich, die Ursachen der Erkrankung zu identifizieren und zu bekämpfen. Unser Ansatz konzentriert sich auf die Wiederherstellung des Gleichgewichts des Mikrobioms, eine entzündungshemmende und nährstoffreiche Ernährung, den Umgang mit psychischem und physischem Stress sowie die Unterstützung und Regulierung des Hormonsystems. Zusammen können diese Maßnahmen dazu beitragen, die Insulinsignalisierung auf zellulärer Ebene zu verbessern und die Stoffwechselfunktionen langfristig zu normalisieren. In diesem Zusammenhang sind Lebensstiländerungen nicht zweitrangig oder optional, sondern von zentraler Bedeutung für den Heilungsprozess. Wenn sie sorgfältig und konsequent umgesetzt werden, stärken sie die körpereigenen Regenerationskräfte und unterstützen eine echte Genesung.
Suchen Sie nach den Ursachen Ihrer Beschwerden?
Der funktionelle Ansatz hilft Ihnen zu verstehen, was hinter Ihren Beschwerden steckt — und liefert einen persönlichen Plan, damit Sie sich wieder wohlfühlen.
Beratung buchenQuellen
47 quellenLiteraturverzeichnis
[1] L. B. Thingholm et al., ‘Obese Individuals with and without Type 2 Diabetes Show Different Gut Microbial Functional Capacity and Composition’, Cell Host Microbe, vol. 26, no. 2, pp. 252-264.e10, Aug. 2019, DOI: https://doi.org/10.1016/j.chom.2019.07.004
[2] ‘Inzulin’, WikipédiaOct. 24, 2024, https://hu.wikipedia.org/w/index.php?title=Inzulin&oldid=27540767
[3] C. Tello, ‘7 Benefits of Insulin & 2 Negative Effects’, SelfHacked, Dec. 18, 2019 https://selfhacked.com/blog/insulin-101/
[4] M. Trovati, P. Massucco, L. Mattiello, E. Mularoni, F. Cavalot, and G. Anfossi, ‘Insulin increases guanosine-3’,5’-cyclic monophosphate in human platelets. A mechanism involved in the insulin anti-aggregating effect’, Diabetes.., vol. 43, no. 8, pp. 1015–1019, 1994, DOI: https://doi.org/10.2337/diab.43.8.1015
[5] O. Farooq and J. I. Isenberg, ‘Effect of continuous intravenous infusion of insulin versus rapid intravenous injection of insulin on gastric acid secretion in man’, Gastroenterology, vol. 68, no. 4 Pt 1, pp. 683–686, Apr. 1975 https://pubmed.ncbi.nlm.nih.gov/1123136/
[6] W. Zarzycki, ‘[Hydrochloric acid, pepsin and mucus secretion in the stomach of healthy probands following a single insulin administration with simultaneous pentagastrin infusion]’, Dtsch. Z. Verdau. Stoffwechselkr., vol. 48, no. 5, pp. 229–238, 1988 https://pubmed.ncbi.nlm.nih.gov/2472262/
[7] J. Wahren, B. L. Johansson, and H. Wallberg-Henriksson, ‘Does C-peptide have a physiological role?’, Diabetologia, vol. 37 Suppl 2, pp. S99-107, Sept. 1994, DOI: https://doi.org/10.1007/BF00400832
[8] D. Semo, H. Reinecke, and R. Godfrey, ‘Gut microbiome regulates inflammation and insulin resistance: a novel therapeutic target to improve insulin sensitivity’, Signal Transduct. Target. Ther., vol. 9, no. 1, p. 35, Feb. 2024, DOI: https://doi.org/10.1038/s41392-024-01746-y
[9] ‘What Is Insulin Resistance?’, Cleveland Clinic https://my.clevelandclinic.org/health/diseases/22206-insulin-resistance
[10] A. M. Freeman, L. A. Acevedo, and N. Pennings, ‘Insulin Resistance’, in StatPearls, Treasure Island (FL): StatPearls Publishing, 2025 https://www.ncbi.nlm.nih.gov/books/NBK507839/
[11] Ede K., István B., Tenno D., Gergely D., and István K., ‘A metabolikus szindróma „Magyarország Átfogó Egészségvédelmi Szûrôprogramja 2010–2020” 2010–2012. évi tevékenységének tükrében’ https://egeszsegprogram.eu/content/kozerdeku-adatok/pdf/publikaciok/hypertonia_es_nephrologia_-_a_metabolikus_szindroma_elemzese_(2013).pdf
[12] ‘2015’ https://ime.memt.hu/wp-content/uploads/2775_48_53.pdf
[13] S. E. Kahn, R. L. Hull, and K. M. Utzschneider, ‘Mechanisms linking obesity to insulin resistance and type 2 diabetes’, Nature, vol. 444, no. 7121, pp. 840–846, 2006, DOI: https://doi.org/10.1038/nature05482
[14] B. K. Pedersen and M. A. Febbraio, ‘Muscles, exercise and obesity: skeletal muscle as a secretory organ’, Nat. Rev. Endocrinol., vol. 8, no. 8, pp. 457–465, Apr. 2012, DOI: https://doi.org/10.1038/nrendo.2012.49
[15] H. Gábor, 2. Energiatermelés az emberi szervezetben | Sportélettan. https://psycho.unideb.hu/sportpszichodiagnosztika/fejezetek/hg_sportelettan/_book/energiatermel%C3%A9s-az-emberi-szervezetben.html
[16] M. Esteve Ràfols, ‘Adipose tissue: cell heterogeneity and functional diversity’, Endocrinol. Nutr. Organo Soc. Espanola Endocrinol. Nutr., vol. 61, no. 2, pp. 100–112, Feb. 2014, DOI: https://doi.org/10.1016/j.endonu.2013.03.011
[17] K. N. Frayn, ‘Visceral fat and insulin resistance--causative or correlative?’, Br. J. Nutr., vol. 83 Suppl 1, pp. S71-77, Mar. 2000, DOI: https://doi.org/10.1017/s0007114500000982
[18] S. R. Preis et al., ‘Abdominal subcutaneous and visceral adipose tissue and insulin resistance in the Framingham heart study’, Obes. Silver Spring Md, vol. 18, no. 11, pp. 2191–2198, 2010, DOI: https://doi.org/10.1038/oby.2010.59
[19] Q. Zhang et al., ‘Overnutrition Induced Cognitive Impairment: Insulin Resistance, Gut-Brain Axis, and Neuroinflammation’, Front. Neurosci., vol. 16, p. 884579, July 2022, DOI: https://doi.org/10.3389/fnins.2022.884579
[20] ‘Kohlenhydratstoffwechsel einfach erklärt’, edubily GmbH https://edubily.de/blogs/ratgeber/kohlenhydratstoffwechsel-einfach-erklart
[21] Sándor D. S., ‘Pharma Online - Inzulinrezisztencia: tények és tévhitek’, Pharma Online, Apr. 05, 2024 https://pharmaonline.hu/cikk/inzulinrezisztencia-tenyek-es-tevhitek
[22] T. V. Rohm, D. T. Meier, J. M. Olefsky, and M. Y. Donath, ‘Inflammation in obesity, diabetes, and related disorders’, Immunity, vol. 55, no. 1, pp. 31–55, Jan. 2022, DOI: https://doi.org/10.1016/j.immuni.2021.12.013
[23] K. Sharma, S. Akre, S. Chakole, and M. B. Wanjari, ‘Stress-Induced Diabetes: A Review’, Cureus, vol. 14, no. 9, p. e29142, DOI: https://doi.org/10.7759/cureus.29142
[24] ‘Shortening Sleep Time Increases Diabetes Risk in Women | Columbia University Irving Medical Center’ https://www.cuimc.columbia.edu/news/shortening-sleep-time-increases-diabetes-risk-women
[25] I. D. Iyegha, A. Y. Chieh, B. M. Bryant, and L. Li, ‘Associations between poor sleep and glucose intolerance in prediabetes’, Psychoneuroendocrinology, vol. 110, p. 104444, 2019, DOI: https://doi.org/10.1016/j.psyneuen.2019.104444
[26] T. Singh et al., ‘Does Insufficient Sleep Increase the Risk of Developing Insulin Resistance: A Systematic Review’, Cureus, vol. 14, no. 3, p. e23501, DOI: https://doi.org/10.7759/cureus.23501
[27] ‘Gut microbial carbohydrate metabolism contributes to insulin resistance | Nature’https://www.nature.com/articles/s41586-023-06466-x
[28] ‘Biokemia_GYTK_szenhidrat_2014.pdf’ http://www.biochem.szote.u-szeged.hu/tartalom/magyar/pdf/Cooscpace_lecture%20handouts_GYTK/Biokemia_GYTK_szenhidrat_2014.pdf
[29] R. J. Perry et al., ‘Acetate mediates a microbiome–brain–β-cell axis to promote metabolic syndrome’, Nature, vol. 534, no. 7606, pp. 213–217, June 2016, DOI: https://doi.org/10.1038/nature18309
[30] L. Crudele, R. M. Gadaleta, M. Cariello, and A. Moschetta, ‘Gut microbiota in the pathogenesis and therapeutic approaches of diabetes’, eBioMedicine, vol. 97, p. 104821, Oct. 2023, DOI: https://doi.org/10.1016/j.ebiom.2023.104821
[31] J. Kim, Y. Wei, and J. R. Sowers, ‘Role of Mitochondrial Dysfunction in Insulin Resistance’, Circ. Res., vol. 102, no. 4, pp. 401–414, Feb. 2008, DOI: https://doi.org/10.1161/CIRCRESAHA.107.165472
[32] S. Jin and S. Diano, ‘Mitochondrial Dynamics and Hypothalamic Regulation of Metabolism’, Endocrinology, vol. 159, no. 10, pp. 3596–3604, Oct. 2018, DOI: https://doi.org/10.1210/en.2018-00667
[33] J. A. Maassen et al., ‘Mitochondrial diabetes: molecular mechanisms and clinical presentation’, Diabetes.., vol. 53 Suppl 1, pp. S103-109, Feb. 2004, DOI: https://doi.org/10.2337/diabetes.53.2007.s103
[34] Halmos T. and Suba I., ‘Mitochondrialis diszfunkció okozta betegségek’, Orv. Hetil., vol. 163, no. 35, pp. 1383–1393, Aug. 2022, DOI: https://doi.org/10.1556/650.2022.32552
[35] U. Siegenthaler, ‘Stable Hydrogen and Oxygen Isotopes in the Water Cycle’, in Lectures in Isotope Geology, Berlin, Heidelberg, 1979, pp. 264–273, DOI: https://doi.org/10.1007/978-3-642-67161-6_22
[36] S. Seneff and A. M. Kyriakopoulos, ‘Cancer, deuterium, and gut microbes: A novel perspective’, Endocr. Metab. Sci., vol. 17, p. 100215, Mar. 2025, DOI: https://doi.org/10.1016/j.endmts.2025.100215
[37] W. C. Knowler et al., ‘Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin’, N. Engl. J. Med., vol. 346, no. 6, pp. 393–403, Feb. 2002, DOI: https://doi.org/10.1056/NEJMoa012512
[38] C. Argano, L. Mirarchi, S. Amodeo, V. Orlando, A. Torres, and S. Corrao, ‘The Role of Vitamin D and Its Molecular Bases in Insulin Resistance, Diabetes, Metabolic Syndrome, and Cardiovascular Disease: State of the Art’, Int. J. Mol. Sci., vol. 24, no. 20, p. 15485, Oct. 2023, DOI: https://doi.org/10.3390/ijms242015485
[39] G. Muscogiuri, S. Palomba, A. S. Laganà, and F. Orio, ‘Inositols in the Treatment of Insulin-Mediated Diseases’, Int. J. Endocrinol., vol. 2016, p. 3058393, 2016, DOI: https://doi.org/10.1155/2016/3058393
[40] P. J. Havel, ‘A scientific review: the role of chromium in insulin resistance’, Diabetes Educ., vol. Suppl, pp. 2–14, 2004 https://pubmed.ncbi.nlm.nih.gov/15208835/
[41] B. Qin, K. S. Panickar, and R. A. Anderson, ‘Cinnamon: Potential Role in the Prevention of Insulin Resistance, Metabolic Syndrome, and Type 2 Diabetes’, J. Diabetes Sci. Technol., vol. 4, no. 3, pp. 685–693, May 2010, DOI: https://doi.org/10.1177/193229681000400324
[42] E. Jablonska et al., ‘The Effect of Selenium Supplementation on Glucose Homeostasis and the Expression of Genes Related to Glucose Metabolism’, Nutrients, vol. 8, no. 12, p. 772, Dec. 2016, DOI: https://doi.org/10.3390/nu8120772
[43] K. J. C. Cruz, J. B. S. Morais, A. R. S. de Oliveira, J. S. Severo, and D. do N. Marreiro, ‘The Effect of Zinc Supplementation on Insulin Resistance in Obese Subjects: a Systematic Review’, Biol. Trace Elem. Res., vol. 176, no. 2, pp. 239–243, Apr. 2017, DOI: https://doi.org/10.1007/s12011-016-0835-8
[44] Erzsébet E., ‘Mitokondriumok’, HealWays, July 12, 2021 https://www.healways.hu/mitokondriumok