Morbus Crohn: Ursachen, Symptome und integrative Therapieansätze

Was ist Morbus Crohn?
Morbus Crohn ist eine entzündliche Darmerkrankung (IBD), die Bauchschmerzen, schweren Durchfall, chronische Müdigkeit, Gewichtsverlust und Unterernährung verursachen kann. Die Entzündung kann verschiedene Teile des Verdauungstrakts betreffen (am häufigsten den Endabschnitt des Dünndarms oder den Dickdarm) und sich sogar auf die tieferen Schichten der Darmwand ausbreiten. Diese Erkrankung kann äußerst schmerzhaft sein und die Lebensqualität beeinträchtigen. In schwereren Fällen können lebensbedrohliche Komplikationen auftreten. Die Ursachen von Morbus Crohn, die Risikogruppen und die wirksamsten Behandlungsmethoden sind noch nicht vollständig geklärt. Trotz bedeutender Fortschritte in den letzten Jahrzehnten gibt es derzeit keine Heilung. Daher sind weitere Forschungsarbeiten erforderlich. Obwohl keine Heilung bekannt ist, können verschiedene Therapien die Symptome lindern und sogar zu einer langfristigen Remission und Heilung der Entzündung führen. Mit einer geeigneten Behandlung kann die Lebensqualität der Patienten erheblich verbessert werden. 1 Der funktionelle medizinische Ansatz bei Morbus Crohn besteht darin, die zugrunde liegenden Ursachen der Entzündung zu identifizieren und zu behandeln, indem die natürlichen Heilungsprozesse des Körpers unterstützt werden. Praktiker der funktionellen oder integrativen Medizin können Tests auf Nahrungsmittelunverträglichkeiten, Stuhlanalysen und andere individuelle Diagnostikverfahren einsetzen. Diese Tests helfen Ärzten und Patienten, die Ursache der Entzündung zu identifizieren und einen personalisierten Behandlungsplan und eine individuelle Ernährung zu entwickeln.
Was sind die Symptome von Morbus Crohn?
Viele Menschen mit Morbus Crohn leiden jahrelang an Symptomen, bevor sie eine offizielle Diagnose erhalten 2. Die Symptome treten meist im Teenageralter oder in den Zwanzigern auf, obwohl die Krankheit in jedem Alter auftreten kann 3. Morbus Crohn verläuft in der Regel schwankend, mit abwechselnden Schüben und Remissionsphasen. 4 Die Symptome entwickeln sich in der Regel allmählich, obwohl in seltenen Fällen auch ein plötzlicher Ausbruch möglich ist. Bestimmte Symptome können sich mit der Zeit verschlimmern. Häufige Frühsymptome sind 5:
- Durchfall
- Bauchkrämpfe
- Blutiger Stuhl
- Fieber
- Müdigkeit
- Appetitlosigkeit
- Gewichtsverlust
- Völlegefühl nach dem Stuhlgang
- Häufiger Stuhldrang
Diese Symptome können oft mit einer Lebensmittelvergiftung, Verdauungsstörungen oder Allergien verwechselt werden.

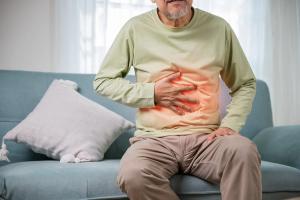
Abbildung 1: Zu den frühesten Symptomen von Morbus Crohn können Bauchschmerzen, Verstopfung, Magenkrämpfe, Gewichtsverlust, Fieber und Müdigkeit gehören
Bauchschmerzen sind eines der häufigsten Frühsymptome von Morbus Crohn 6, insbesondere im rechten Unterbauch. In schweren Fällen können Patienten mehr als 20 Stuhlgänge pro Tag haben und häufig nachts aufwachen, um den Stuhl zu entleeren 3, 6–8. Es kann auch zu blutigem Stuhlgang kommen, der in der Regel sporadisch auftritt und hell- oder dunkelrot sein kann. In fortgeschrittenen Stadien kann es zu starken Blutungen kommen. 9 Mit fortschreitender Erkrankung können sich die Symptome verstärken, darunter 5:
- Rektalfisteln
- Geschwüre (überall vom Mund bis zum Anus)
- Gelenk- und Hautentzündungen
- Atemnot oder eingeschränkte Mobilität aufgrund von Anämie
Eine frühzeitige Erkennung kann helfen, schwerwiegende Komplikationen zu vermeiden und eine rechtzeitige Behandlung zu ermöglichen. Morbus Crohn kann auch Symptome außerhalb des Darmtraktes verursachen, darunter 10:
- Augen (Rötung, Schmerzen, Sehstörungen)
- Mund (Geschwüre)
- Gelenke (Schmerzen und Schwellungen)
- Haut (Knoten, Geschwüre, Wunden, Hautausschläge)
- Knochen (Osteoporose)
- Nieren (Nierensteine)
- Leber (primär sklerosierende Cholangitis und Zirrhose – selten)

Abbildung 2: Symptome im Zusammenhang mit Morbus Crohn können auch außerhalb des Darmtraktes auftreten und andere Teile des Körpers betreffen
Symptome, die außerhalb des Verdauungstraktes auftreten, werden als extraintestinale Manifestationen bezeichnet. Bei manchen treten diese Symptome Jahre vor den Darmbeschwerden auf, bei anderen fallen sie mit Schüben zusammen.
Komplikationen der Morbus Crohn
Zu den Komplikationen können Darmverschluss, Abszesse, Perforationen und Blutungen gehören, die lebensbedrohlich sein können. Morbus Crohn kann auch Organe außerhalb des Verdauungstrakts befallen 11. Eine häufige Komplikation im Bereich der Augen ist die Uveitis, die zu verschwommenem Sehen und Augenschmerzen führen kann 12. Unbehandelt kann sie zur Erblindung führen 11. Entzündungen können sowohl in der Bindehaut als auch in der Lederhaut auftreten, was zu Skleritis oder Episkleritis führen kann. 12 Morbus Crohn steht in Zusammenhang mit einer rheumatischen Erkrankung namens seronegative Spondyloarthritis, die durch Gelenkentzündungen (Arthritis) oder Entzündungen an Sehnenansätzen (Enthesitis) gekennzeichnet ist. 12 Weitere betroffene Systeme sind die Haut, das Blut und das endokrine System. Die häufigste Hauterkrankung ist das Erythema nodosum, von dem etwa 8 % der Patienten betroffen sind. Es verursacht schmerzhafte rote Knoten, meist an den Beinen 12–14. Eine seltenere, aber schwerwiegendere Hauterkrankung ist das Pyoderma gangrenosum, von dem weniger als 2 % der Patienten betroffen sind und das durch schmerzhafte, ulzerierte Knötchen gekennzeichnet sind. 11, 14 Morbus Crohn erhöht auch das Risiko für Blutgerinnsel 12. Beinschmerzen und Schwellungen können auf eine tiefe Venenthrombose hindeuten, während plötzliche Atemnot auf eine Lungenembolie hinweisen könnte. Neurologische Komplikationen treten bei bis zu 15 % der Patienten auf, darunter Krampfanfälle, Schlaganfälle, Muskelerkrankungen (Myopathie), periphere Neuropathie, Kopfschmerzen und Depressionen. 15 Aufgrund der anhaltenden Entzündung kann Morbus Crohn das Krebsrisiko erhöhen. Eine Beteiligung des Dünndarms ist mit einem höheren Risiko für Dünndarmkrebs verbunden 16, während eine Beteiligung des Dickdarms das Risiko für Darmkrebs erhöht. 17 Morbus Crohn verursacht häufig Anämie, die auf einen Mangel an Vitamin B12, Folsäure oder Eisen oder auf chronische Entzündungen zurückzuführen sein kann 18–19. Die Erkrankung betrifft häufig das terminale Ileum, wo Vitamin B12 resorbiert wird 18, was erklärt, warum ein Mangel besonders häufig nach der operativen Entfernung dieses Abschnitts auftritt. 19
Was verursacht Morbus Crohn?
Obwohl die genauen Ursachen unbekannt sind, resultiert Morbus Crohn wahrscheinlich aus einer Kombination von genetischen, immunologischen, mikrobiellen und umweltbedingten Faktoren bei genetisch prädisponierten Personen 6, 20–22. Daher können die unten aufgeführten Ursachen – Genetik, Faktoren des Immunsystems, Krankheitserreger und Umwelteinflüsse – alle zur Entstehung der Krankheit beitragen. Es wurde kein einzelner Faktor als alleinige Ursache identifiziert.
Genetik
Es wird angenommen, dass Morbus Crohn durch eine genetische Veranlagung in Kombination mit Umweltauslösern entsteht 23. Es ist die erste genetisch komplexe Krankheit, bei der die Zusammenhänge zwischen genetischen Faktoren und dem Immunsystem umfassend untersucht wurden 24. Über 70 Gene wurden mit Morbus Crohn in Verbindung gebracht, wobei die Genetik etwa die Hälfte des Gesamtrisikos ausmacht. 3, 25
Genomische Studien zeigen genetische Überschneidungen zwischen IBD und Zöliakie 26. Morbus Crohn steht auch in Zusammenhang mit dem LRRK2-Gen, das mit der Parkinson-Krankheit assoziiert ist. 27
Immunsystem
Morbus Crohn wird allgemein als Autoimmunerkrankung angesehen. Einige Theorien gehen jedoch von Defekten im angeborenen Immunsystem aus 28. Eine Hypothese besagt, dass eine Fehlfunktion der Makrophagen die Zytokinsekretion beeinträchtigt und eine chronische mikrobielle Entzündung auslöst 21, 29. Eine andere Hypothese geht davon aus, dass die Entzündung auf übermäßige Th1- und Th17-Immunreaktionen zurückzuführen ist. 30–31
Eine Theorie geht davon aus, dass sich das Immunsystem in Gegenwart von Parasiten entwickelt hat; durch die moderne Hygiene könnte eine geringere Exposition die Immunregulation schwächen. In einer Studie zeigten 23 von 29 Morbus-Crohn-Patienten, die harmlosen Parasiten ausgesetzt waren, eine Verbesserung der Symptome, wobei 21 eine Remission erreichten. 32
Krankheitserreger
Obwohl die genauen Ursachen der Crohn-Krankheit nach wie vor unbekannt sind, deuten immer mehr Forschungsergebnisse darauf hin, dass neben der genetischen Veranlagung auch verschiedene Mikroorganismen – darunter Krankheitserreger – eine Rolle bei der Entstehung der Erkrankung spielen könnten. Aktuelle Theorien gehen davon aus, dass Morbus Crohn bei Personen auftritt, die eine abnormale Immunantwort auf die Darmmikrobiota entwickeln 33. Diese Immundysregulation kann durch eine vorangegangene Infektion, wie z. B. eine Gastroenteritis, oder durch eine Störung des mikrobiellen Gleichgewichts (Homöostase), bekannt als Dysbiose, ausgelöst werden. 3
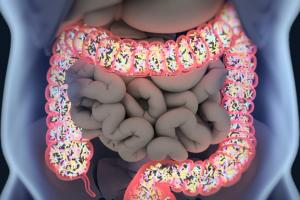
Mikrobiom
Das Darmmikrobiom – bestehend aus der gesamten Bandbreite an Mikroorganismen, vor allem Bakterien, die den Verdauungstrakt besiedeln – spielt eine wichtige Rolle bei der Aufspaltung und Aufnahme von Nährstoffen, der Regulierung des Immunsystems und der Aufrechterhaltung der Integrität der Darmschleimhaut. Bei Menschen mit Morbus Crohn ist dieses mikrobielle Gleichgewicht gestört: Die Vielfalt nimmt ab und das Verhältnis verschiebt sich weg von nützlichen Bakterien. Bemerkenswerte entzündungshemmende Arten wie Faecalibacterium prausnitzii, Bifidobacterium und Lactobacillus zeigen eine deutliche Abnahme ihrer Häufigkeit 34. Gleichzeitig steigt der Anteil potenziell pathogener Bakterien, insbesondere von Mitgliedern der Proteobacteria-Gruppe wie Escherichia coli und Shigella dysenteriae. 35–36
Besondere Aufmerksamkeit gilt den adhärenten invasiven E. coli (AIEC)-Stämmen, die sich an Darmepithelzellen anheften, in diese eindringen und sich in Makrophagen vermehren können, wodurch sie die Entzündungsreaktion verstärken 37. Forschungsergebnisse deuten darauf hin, dass AIEC-Stämme bei etwa einem Drittel der Morbus-Crohn-Patienten vorhanden sind 38. Darüber hinaus stehen Veränderungen in der Zusammensetzung des Mikrobioms nicht nur mit dem Vorliegen der Erkrankung in Zusammenhang, sondern auch mit deren Schweregrad. So sind beispielsweise Alistipes shahii und Pseudodesulfovibrio aespoeensis mit einer geringeren Entzündungsaktivität verbunden, während Polynucleobacter wianus mit einer erhöhten Entzündung und einem schwereren Krankheitsverlauf korreliert.
Neuere Studien deuten darauf hin, dass bestimmte von Alistipes shahii produzierte Metaboliten sogar antitumorale Eigenschaften aufweisen können. In ähnlicher Weise scheint Akkermansia muciniphila eine immunmodulatorische Wirkung auszuüben, indem es durch die Aktivierung von IL-10-produzierenden regulatorischen T-Zellen die Konzentrationen von inflammatorischen Zytokinen und Chemokinen – darunter TNF-α, IL-1β und IL-6 – senkt. Im Gegensatz dazu neigen opportunistische Pathogene wie Morganella morganii und Proteus mirabilis dazu, unter dysbiotischen Bedingungen zu gedeihen und Entzündungen durch Schädigung der Darmschleimhaut aufrechtzuerhalten. Besonders besorgniserregend ist M. morganii, das durch die Produktion von Indolinen, die die DNA schädigen, zur Entstehung von Darmkrebs beitragen kann. 39
Es ist wichtig zu beachten, dass ein Ungleichgewicht des Mikrobioms nicht nur eine Folge von Entzündungen ist, sondern auch aktiv zu deren Entstehung und Fortdauer beitragen kann. Diese Erkenntnis hat neue therapeutische Strategien eröffnet, darunter die Verwendung von Probiotika, Präbiotika, Mikrobiomtransplantationen und mikrobiota-modulierenden Pflanzenstoffen.
Andere Mikroorganismen
Neben Darmbakterien wurden mehrere andere Mikroorganismen als potenzielle unabhängige Krankheitserreger identifiziert. Aktuelle Erkenntnisse deuten auf Mycobacterium avium subspecies paratuberculosis (MAP), bestimmte E. coli-Stämme (z. B. AIEC), das Epstein-Barr-Virus (EBV), Candida tropicalis und Clostridioides difficile als mögliche Verursacher hin. Diese Krankheitserreger können die Darmschleimhaut direkt schädigen und unangemessene oder übermäßige Immunreaktionen hervorrufen, wodurch sie sowohl bei der Entstehung als auch beim chronischen Fortbestehen von Morbus Crohn eine Rolle spielen. Mycobacterium avium subspecies paratuberculosis (MAP) MAP verursacht die Johne-Krankheit im Darm von Rindern. Da die Johne-Krankheit Ähnlichkeiten mit Morbus Crohn aufweist, wird angenommen, dass dieses Bakterium auch bei Morbus Crohn eine Rolle spielen könnte. In mehreren Studien wurde die Beteiligung von MAP an der Entstehung von Morbus Crohn untersucht. 40–41 Die Ausrottung von MAP wird auch als therapeutischer Ansatz untersucht 42. So wurde beispielsweise eine Antibiotikabehandlung gegen MAP untersucht. Obwohl die Ergebnisse noch nicht eindeutig sind, wird der Einsatz von Antibiotika allgemein als vorteilhaft angesehen. 43–44 Escherichia coli Da adhärente invasive Escherichia coli (AIEC) bei Personen mit Morbus Crohn häufiger vorkommen, wurden bestimmte Stämme von AIEC mit der Krankheit in Verbindung gebracht 37, 45–46. Diese Bakterien sind in der Lage, stärkere Biofilme zu bilden als nicht-adhärente invasive E. coli-Stämme. 47–48 Epstein-Barr-Virus Das Epstein-Barr-Virus steht in engem Zusammenhang mit mehreren Darmerkrankungen. Neben Morbus Crohn wurde es auch mit Colitis ulcerosa, Magengeschwüren, akuter Blinddarmentzündung und Magenkrebs in Verbindung gebracht. Das Virus wird in gesunder Magen-Darm-Schleimhaut nicht nachgewiesen, ist jedoch in 55 % bis 63 % der Darm-Gewebeproben von Personen mit Morbus Crohn vorhanden. 49–50 Besonders besorgniserregend ist, dass das Epstein-Barr-Virus inaktiv bleiben kann, bis es durch immunsuppressive Medikamente wie Steroide reaktiviert wird 51. Folglich können diese Medikamente Morbus Crohn weiter verschlimmern. 52 Candida tropicalis Eine 2016 in der Zeitschrift der American Society for Microbiology veröffentlichte Studie berichtete über eine erhöhte Inzidenz von Candida tropicalis im Stuhl von Patienten mit Morbus Crohn. Hohe Konzentrationen dieses Pilzes wurden auch zusammen mit Antikörpern gegen Saccharomyces cerevisiae gefunden, was eine Möglichkeit bietet, Morbus Crohn von Colitis ulcerosa zu unterscheiden. Diese Pilze wurden zusammen mit zwei Bakterien, Escherichia coli und Serratia marcescens, entdeckt. Zusammen bildeten der Pilz und die beiden Bakterien einen dicken, großen Biofilm. Diese Biofilme trugen zur Dysbiose der Darmflora bei Morbus Crohn bei. Diese Studie war die erste, die zeigte, dass auch Pilze eine ursächliche Rolle bei Morbus Crohn spielen können, während zuvor nur Bakterien und Viren verdächtigt wurden. 33 Clostridioides difficile Clostridium difficile ist ein häufiger Bewohner des Darmtraktes, wobei sich mehrere Stämme in ihrer Pathogenität unterscheiden. Seine Anwesenheit deutet nicht unbedingt auf eine Erkrankung hin. Eine Antibiotikabehandlung stört oft die Darmflora, was zu Durchfall und einer Infektion mit Clostridium difficile führen kann. 53 Clostridium-Infektionen spielen auch eine bedeutende Rolle bei entzündlichen Darmerkrankungen. 54 Clostridium difficile ist eine häufige nosokomiale Infektion mit einer Sterblichkeitsrate zwischen 8 % und 37,2 % laut Forschungsergebnissen 55. Das Infektionsrisiko wurde um 50 % reduziert, wenn Probiotika gleichzeitig mit Antibiotika verabreicht wurden. 56
Umwelteinflüsse
Morbus Crohn tritt häufiger in westlichen Ländern auf 57 und betrifft 3,2 von 1.000 Menschen in Europa und Nordamerika 58, ist jedoch in Asien und Afrika seltener anzutreffen. 58–59 Er beginnt in der Regel im Jugendalter oder im frühen Erwachsenenalter 3, 6, 60 und betrifft beide Geschlechter gleichermaßen. 6 Morbus Crohn steht in Zusammenhang mit einer hohen Aufnahme von tierischen Proteinen und Milchproteinen sowie einem erhöhten Verhältnis von Omega-6- zu Omega-3-Fettsäuren. Bei Menschen, die pflanzliche Proteine zu sich nehmen, tritt die Krankheit seltener auf. Fischproteine zeigen keine Wirkung. 61 Bei Rauchern ist das Risiko, an Morbus Crohn zu erkranken, doppelt so hoch wie bei Nichtrauchern. Darüber hinaus erhöht Rauchen das Risiko eines Rückfalls und von Schüben bei bereits diagnostizierten Patienten weiter. 62 Die Einführung hormoneller Verhütungsmittel in den Vereinigten Staaten in den 1960er Jahren fiel mit einem signifikanten Anstieg der Morbus-Crohn-Erkrankungen zusammen. Eine Hypothese besagt, dass diese Medikamente das Verdauungssystem in ähnlicher Weise beeinflussen wie Rauchen 58. Es wird auch angenommen, dass chronischer Stress die Krankheit verschlimmert, obwohl konkrete Beweise dafür fehlen. 6
Risikofaktoren
Die folgenden Faktoren können zum Ausbruch von Morbus Crohn beitragen 1:
- Alter: Obwohl Morbus Crohn in jedem Alter auftreten kann, beginnt er am häufigsten im jungen Erwachsenenalter. Die meisten Menschen werden vor dem 30. Lebensjahr diagnostiziert.
- Ethnische Zugehörigkeit: Obwohl Morbus Crohn jede ethnische Gruppe betreffen kann, tritt er am häufigsten bei Kaukasiern auf.
- Genetik: Personen mit einem Verwandten ersten Grades (Eltern, Geschwister oder Kinder), der an Morbus Crohn leidet, haben ein deutlich höheres Risiko. Etwa 20 % der Morbus-Crohn-Patienten haben einen Familienangehörigen mit dieser Erkrankung.
- Rauchen: Das Aufhören mit dem Rauchen ist der wirksamste veränderbare Risikofaktor zur Vorbeugung von Morbus Crohn.
- Entzündungshemmende Medikamente: Obwohl nichtsteroidale Antirheumatika (NSAR) keinen Morbus Crohn verursachen, können sie zu Darmentzündungen beitragen und den Zustand verschlimmern.

Abbildung 3: Zu den Risikofaktoren für Morbus Crohn können Alter, genetische Faktoren, ethnische Zugehörigkeit und Rauchen gehören
Diagnose von Morbus Crohn
Die Diagnose von Morbus Crohn ist schwierig 2. Oft sind mehrere Tests erforderlich, und selbst dann ist eine definitive Diagnose möglicherweise nicht möglich. 60 Die Diagnose sollte auf der Anamnese, der körperlichen Untersuchung, bildgebenden Verfahren und Labor-Untersuchungsergebnissen basieren. Es ist entscheidend, Morbus Crohn von ähnlichen Erkrankungen wie dem Reizdarmsyndrom (IBS), der Behçet-Krankheit oder Infektionskrankheiten wie Yersiniose und Enteroviren zu unterscheiden. Endemische Krankheiten wie Tuberkulose müssen ebenfalls ausgeschlossen werden. 3 Die folgenden Diagnosewerkzeuge können verwendet werden, um Morbus Crohn zu bestätigen, ihn von anderen Erkrankungen wie IBS und Colitis ulcerosa zu unterscheiden und andere Ursachen auszuschließen 3:
- Die Anamnese, einschließlich einer detaillierten Familienanamnese, ist unerlässlich. Dabei sollten Faktoren wie der Zeitpunkt des Auftretens der Symptome, kürzlich unternommene Reisen, das Vorhandensein von Blut und/oder Schleim im Stuhl, Krämpfe, nächtlicher Durchfall, Essgewohnheiten, kürzlich aufgetretene Darminfektionen, die Einnahme nichtsteroidaler Antirheumatika, eine Blinddarmoperation in der Vorgeschichte und kürzlich aufgetretene Episoden von Gastroenteritis berücksichtigt werden. Darüber hinaus ist eine Untersuchung auf Symptome außerhalb des Darmtraktes erforderlich.
- Körperliche Untersuchung: Umfasst Puls, Blutdruck, Gewicht, BMI, Untersuchung des Abdomens und des Perianalbereichs, digitale rektale Untersuchung und Überprüfung auf extraintestinale Anzeichen.
- Mikrobiologische Tests: Stuhlanalyse und Test auf Clostridium difficile.
- Pathologische und histologische Analyse: Mindestens zwei Biopsien aus fünf Darmabschnitten, einschließlich des Ileums.
- Gastroskopie
- Koloskopie
- Dünndarmendoskopie
- Röntgen
- CT
- MR
- Kapselendoskopie
- Laboruntersuchungen: Großes Blutbild, Blutsenkungsgeschwindigkeit, C-reaktives Protein, Leberwerte, Elektrolyte und Antikörperscreening (ASCA = Hefe-Antikörper, ANCA = antineutrophile zytoplasmatische Antikörper).
- Patienten mit vermuteten oder bestätigten extraintestinalen Symptomen sollten auch Spezialisten wie Chirurgen, Rheumatologen, Dermatologen, Augenärzte, Urologen oder Gynäkologen (bei Verdacht auf eine rektovaginale Fistel) konsultieren.
Welche Lebensmittel verursachen Symptome?
Lebensmittel und Getränke verursachen keine entzündlichen Darmerkrankungen, können jedoch die Symptome verschlimmern, insbesondere während eines Schubs. 1 Das Führen eines Ernährungstagebuchs kann Patienten dabei helfen, herauszufinden, welche Lebensmittel Symptome auslösen, sodass sie ihre Ernährung entsprechend anpassen können. Viele Patienten stellen fest, dass die Reduzierung oder der Verzicht auf Milchprodukte Durchfall, Bauchschmerzen und Blähungen lindert. Möglicherweise liegt eine Laktoseintoleranz vor, und auch Milchproteine können zu den Symptomen beitragen. Der Verzicht auf Kasein (ein Protein in Kuhmilch) und möglicherweise auch auf Gluten kann ebenfalls hilfreich sein. 64 Eine ballaststoff- und obstreiche Ernährung ist mit einem verringerten Crohn-Risiko verbunden, während eine Ernährung mit hohem Fettanteil, mehrfach ungesättigten Fettsäuren wie Omega-6 und Fleisch das Risiko erhöhen kann. Während Schüben kann eine ballaststoffarme Ernährung helfen, akute Symptome zu lindern. 65
Wie kann Morbus Crohn behandelt werden?
Derzeit gibt es keine Heilung oder chirurgische Behandlung, die Morbus Crohn beseitigen kann 3, 6. Das Ziel der Behandlung ist es, Entzündungen zu reduzieren, Symptome (Schmerzen, Durchfall, Blutungen) zu lindern und Ernährungsdefizite auszugleichen. 66 Die Behandlung kann Medikamente, Nahrungsergänzungsmittel, Operationen oder eine Kombination davon umfassen, je nach Stadium der Erkrankung, Schweregrad, Komplikationen und bisherigen Behandlungserfolgen. Zur Behandlung von Morbus Crohn werden verschiedene Medikamente eingesetzt. Dazu gehören entzündungshemmende Medikamente wie Kortikosteroide, Antibiotika und Medikamente gegen Durchfall. Immunsuppressiva wie Methotrexat oder Azathioprin können ebenfalls verschrieben werden. Zur Linderung der Schmerzen können verschiedene Schmerzmittel eingesetzt werden. In schwereren Fällen kann eine biologische Therapie angewendet werden. Chirurgische Eingriffe können durchgeführt werden, um Komplikationen der Morbus Crohn-Erkrankung zu behandeln, darunter Fisteln, Dünndarmverschluss, Darmkrebs, Dünndarmkrebs und Darmverschlüsse. Eine Operation ist auch notwendig, wenn ein Abschnitt des Darms nicht mehr auf Medikamente anspricht 67. Eine Operation heilt oder beseitigt jedoch nicht die Morbus Crohn-Erkrankung selbst. 68 Müdigkeit kann durch regelmäßige Bewegung, eine ausgewogene Ernährung und ausreichend Schlaf bekämpft werden. Rauchen kann die Symptome verschlimmern, daher wird dringend empfohlen, mit dem Rauchen aufzuhören. 65 Bei der Stuhltransplantation (FMT) wird Stuhl von einem gesunden Spender übertragen, um das Darmmikrobiom des Patienten wiederherzustellen. Dieser Ansatz ist vielversprechend und hat nur wenige Nebenwirkungen bei Morbus Crohn und anderen IBDs. 69–70
Funktionalmedizinischer Ansatz
Wie bei anderen integrativen Ansätzen zur Behandlung von Autoimmunerkrankungen zielt auch die funktionelle Behandlung von Morbus Crohn darauf ab, die Ursachen der Entzündung aufzudecken und zu bekämpfen.
Ein integrativer Arzt kann Tests auf Nahrungsmittelunverträglichkeiten und eine Stuhlanalyse anordnen. Mithilfe dieser Instrumente kann er gemeinsam mit dem Patienten die zugrunde liegenden Ursachen der Entzündung identifizieren. Mögliche Auslöser oder verschlimmernde Faktoren können bestimmte Lebensmittel, Ungleichgewichte in der Darmflora, Bakterien, Pilze, Parasiten, Viren, das Leaky-Gut-Syndrom oder ein Mangel an nützlichen Darmbakterien sein. Auf der Grundlage personalisierter, patientenspezifischer Tests können integrative Ärzte einen maßgeschneiderten Behandlungsplan entwickeln, der den Schwerpunkt auf Ernährung, Nahrungsergänzungsmittel, Bewegung und in einigen Fällen auch Meditation legt. 71
Empfohlene Diäten sind: Spezifische Kohlenhydratdiät (SCD), Eliminationsdiät. Beide konzentrieren sich darauf, symptomauslösende Lebensmittel zu entfernen und nährstoffreiche Optionen in den Vordergrund zu stellen. 71
Mehrere Nahrungsergänzungsmittel können ebenfalls bei der Behandlung von Morbus Crohn wirksam sein. Dazu gehören in erster Linie entzündungshemmende Wirkstoffe wie Omega-3-Fettsäuren und Produkte auf Kurkuma-Basis. Zinkglycinat, N-Acetylglucosamin und Vitamin D3 können zur Wiederherstellung der Darmflora beitragen. 71
Dr. Lums Plan für Morbus Crohn und Colitis ulcerosa
Dies ist kein Ersatz für eine akute/notfallmäßige Behandlung, sondern konzentriert sich auf die Bekämpfung der Ursachen und die Förderung der Heilung 72:
Dieser Ansatz konzentriert sich sowohl auf genetische Faktoren als auch auf die Behandlung zugrunde liegender Infektionen.
Schritt 1: Wiederherstellung der Verdauung
Salzsäure: Es ist wichtig, die natürliche Fähigkeit des Magens wiederherzustellen, ausreichende Mengen an Salzsäure zu produzieren, um die Verdauung zu unterstützen. Dazu gehört die Unterstützung der Heilung und Regeneration der für die Säureproduktion verantwortlichen Gewebe und Zellen.
Pankreasenzyme: Diese Verdauungsenzyme sind für die Aufspaltung und Aufnahme von Nahrung unerlässlich. Es reicht nicht aus, nur die Enzyme zu ersetzen – auch die Bauchspeicheldrüse selbst muss behandelt und geheilt werden. Das ultimative Ziel ist es, die Verdauung so wiederherzustellen, dass sie ohne zusätzliche Enzyme funktioniert.
Galle: Entzündliche Darmerkrankungen stören häufig die Gallenproduktion und den Gallenfluss. Ein häufiges Anzeichen dafür sind Verdauungsprobleme nach dem Verzehr fettiger Speisen. Eine ordnungsgemäße Gallenfunktion ist entscheidend für den Fettabbau und die Aufnahme fettlöslicher Vitamine (A, E, K und Vitamin D).
Stuhlgang: Unabhängig davon, ob Verstopfung oder Durchfall vorliegt, ist das Ziel der Behandlung die Wiederherstellung eines ausgeglichenen Stuhlgangs, damit die Verdauung weder zu langsam noch zu schnell erfolgt.
Schritt 2: Wiederherstellung des Mikrobioms und Behandlung von Infektionen
Das Mikrobiom hat einen direkten Einfluss auf die Schwere von Entzündungen, die Gesundheit des Immunsystems und die Verdauung insgesamt. Die Funktionsanalyse des Darmmikrobiota spielt eine entscheidende Rolle bei der Genesung. Die Identifizierung und Behandlung latenter Infektionen ist für eine langfristige Linderung der Symptome unerlässlich.
Schritt 3: Identifizierung genetischer Veranlagungen
Genetische Faktoren können Entzündungen verschlimmern oder das Gleichgewicht der Neurotransmitter (Serotonin, Dopamin) beeinflussen. Die Identifizierung dieser Faktoren hilft bei der individuellen Anpassung der Genesungsstrategien.
Schritt 4: Beurteilung der Leberfunktion
Die Mehrheit der Menschen mit entzündlichen Darmerkrankungen hat zugrunde liegende Leberprobleme. Herkömmliche Tests reichen jedoch oft nicht aus, um Leberprobleme vollständig auszuschließen. Eine erkrankte Leber kann zu Funktionsstörungen des Darmtraktes beitragen. Die Unterstützung der Lebergesundheit und -funktion kann die Heilung des Darmtraktes beschleunigen.
Bei entzündlichen Darmerkrankungen greift das Immunsystem des Körpers schädliche Mikroben wie Viren, Bakterien, Pilze und Parasiten an und versucht, sie zu eliminieren. Diese Immunreaktion führt zu den für diese Erkrankungen charakteristischen chronischen Entzündungen.
Wenn das Mikrobiom gestört ist, wird das Abwehrsystem des Körpers geschwächt, sodass sich Infektionen ansammeln können. Das Immunsystem verstärkt dann seine Bemühungen, diese Krankheitserreger zu bekämpfen, was weitere Entzündungen auslöst.
Dieser Teufelskreis verschlimmert die Symptome von Morbus Crohn. Diese Symptome treten in der Regel zyklisch auf, da verschiedene Faktoren die Gesundheit des Immunsystems und die Schwere der Entzündung beeinflussen.
Faktoren wie chronischer Schlafmangel, Nahrungsmittelallergien, der Verzehr von verarbeiteten Lebensmitteln und Stress können die Symptome verschlimmern und die Immunfunktion schwächen. Daher zielt die Behandlung darauf ab, das Immunsystem zu stärken, indem das Gleichgewicht des Darmmikrobiota wiederhergestellt und zugrunde liegende versteckte Infektionen behandelt werden.
Die Lösung:
Das Ziel ist es, die Neurotransmitter Serotonin und Dopamin sowohl im Gehirn als auch im Magen-Darm-System ins Gleichgewicht zu bringen. Wenn diese beiden Neurotransmitter im Gleichgewicht sind, löst ein übermäßiger Serotoninspiegel keine Entzündungsprozesse mehr aus, sodass das Darmgewebe mit der Heilung beginnen kann.
Die Behandlung umfasst den Ersatz von Serotonin- und Dopamin-Vorläufern (Aminosäure Vorläufern) unter ärztlicher Aufsicht. Darüber hinaus ist die Wiederherstellung des Gleichgewichts der Darmflora von entscheidender Bedeutung, wozu die Beseitigung infektiöser Krankheitserreger, die Heilung der Darmwand und die Stärkung des Immunsystems gehören.
Daher umfasst die integrative Behandlung von Morbus Crohn die Behebung festgestellter Nährstoffmängel, die Optimierung der Verdauung und Aufnahme von Nahrungsmitteln und Nährstoffen, die Erreichung einer angemessenen Menge und eines angemessenen Verhältnisses von Darmbakterien, die Entwicklung einer personalisierten Ernährung und die Wiederherstellung einer gesunden Darmflora. Die Behandlung genetischer Defekte, die Neurotransmitter beeinträchtigen, ist einer der wichtigsten Faktoren für die vollständige Remission von entzündlichen Darmerkrankungen.
Ein weiterer Ansatz aus der funktionellen Medizin ist Mullins DIGIN-Modell 73. Dieses Modell bewertet die Gesundheit des Patienten in fünf grundlegenden Bereichen: Verdauung und Resorption, Darmpermeabilität, Entzündungen, Immunsystem und Nervensystem.
Andere verwandte Erkrankungen
Colitis ulcerosa
Die Symptome von Morbus Crohn ähneln denen der Colitis ulcerosa, einer entzündlichen Erkrankung, die auf den Dickdarm beschränkt ist. Beide Erkrankungen werden als entzündliche Darmerkrankungen (IBD) klassifiziert und weisen oft ähnliche Symptome auf. Es ist jedoch wichtig, zwischen den beiden zu unterscheiden, da ihr Verlauf und ihre Behandlung unterschiedlich sein können. Wenn die Erkrankungen nicht eindeutig unterschieden werden können, wird die Diagnose als unbestimmte Colitis bezeichnet. 3, 8–9
Morbus Crohn kann jeden Teil des Magen-Darm-Trakts betreffen, während Colitis ulcerosa in der Regel auf den Dickdarm beschränkt ist 74. Bei Colitis ulcerosa ist die Entzündung im gesamten betroffenen Bereich kontinuierlich, während bei Morbus Crohn die Entzündung segmental ist und an mehreren Stellen auftritt, wobei sich zwischen den entzündeten Abschnitten gesundes Gewebe befindet.
IBD
IBD steht für „inflammatory bowel disease” (entzündliche Darmerkrankung), eine Kategorie, die sowohl Morbus Crohn als auch Colitis ulcerosa umfasst. Laut einer Übersicht aus dem Jahr 2014 ist Morbus Crohn in der Regel schwerwiegender, aber seltener als Colitis ulcerosa. 75
IBS
Das Reizdarmsyndrom (IBS) ist eine häufige Erkrankung, von der etwa 20 % der Bevölkerung betroffen sind. Wie bei IBDs, einschließlich Morbus Crohn, treten die Symptome von IBS in der Regel zyklisch auf. Schübe können mehrere Tage andauern, und die Symptome können sich nach dem Essen verschlimmern. Bei Frauen treten die Symptome häufig während der Menstruation verstärkt auf. 76
IBS ist in der Regel mit abrupten Veränderungen der Stuhlgewohnheiten – Durchfall oder Verstopfung – verbunden und kann mit Symptomen wie den folgenden einhergehen 76:
- Durchfall
- Verstopfung
- Bauchschmerzen
- Krämpfe
- Blähungen und Gas
- laute Darmgeräusche
- Gefühl der unvollständigen Entleerung
- Schleim im Stuhl
Entzündliche Darmerkrankungen (IBD) wie Morbus Crohn und das Reizdarmsyndrom (IBS) haben Gemeinsamkeiten, da beide unheilbar sind. Sie können ähnliche Symptome verursachen, und die Diagnose beider Erkrankungen ist oft ein langwieriger Prozess. Eine weitere Gemeinsamkeit besteht darin, dass sowohl IBS als auch Morbus Crohn chronische Erkrankungen sind, die durch schwankende Symptome gekennzeichnet sind, die zwischen Schüben und Remissionen wechseln. Beide können auch Symptome außerhalb des Verdauungstrakts hervorrufen. 76
Der wesentliche Unterschied besteht darin, dass IBD, einschließlich Morbus Crohn, eine Autoimmunerkrankung ist, während IBS wahrscheinlich durch Verdauungsstörungen und ein Ungleichgewicht in der Darmflora verursacht wird. Im Gegensatz zu Colitis ulcerosa und Morbus Crohn ist IBS keine entzündliche Erkrankung. Medikamente können bei Menschen mit IBD zur Linderung der Symptome beitragen, während die Behandlung von IBS in erster Linie auf Änderungen des Lebensstils und der Ernährung ausgerichtet ist. Darüber hinaus deuten aktuelle Erkenntnisse darauf hin, dass IBS im Gegensatz zu Morbus Crohn das Risiko für Darmkrebs nicht erhöht. 76
Suchen Sie nach den Ursachen Ihrer Beschwerden?
Der funktionelle Ansatz hilft Ihnen zu verstehen, was hinter Ihren Beschwerden steckt — und liefert einen persönlichen Plan, damit Sie sich wieder wohlfühlen.
Beratung buchenQuellen
79 quellenLiteraturverzeichnis
[1] Mayo Clinic Staff, “Crohn’s disease - Symptoms and causes,” Mayo Clinic, 2020 https://www.mayoclinic.org/diseases-conditions/crohns-disease/symptoms-causes/syc-20353304
[2] M. Pimentel et al., “Identification of a prodromal period in Crohn’s disease but not ulcerative colitis,” Am. J. Gastroenterol., vol. 95, no. 12, pp. 3458–3462, 0 2000, DOI: https://doi.org/10.1111/j.1572-0241.2000.03361.x
[3] D. C. Baumgart and W. J. Sandborn, “Crohn’s disease,” Lancet Lond. Engl., vol. 380, no. 9853, pp. 1590–1605, 0 2012, DOI: https://doi.org/10.1016/S0140-6736(12)60026-9
[4] N. R. C. (US) C. on D. and C. of J. Disease, Johne’s Disease and Crohn’s Disease. National Academies Press (US), 2003 https://www.ncbi.nlm.nih.gov/books/NBK207651/
[5] Z. Risoldi Cochrane and K. Holland, “Crohn’s Disease: Causes, Symptoms, Diagnosis, and More,” Healthline, Aug. 22, 2018 https://www.healthline.com/health/crohns-disease
[6] “Crohn’s Disease | NIDDK,” National Institute of Diabetes and Digestive and Kidney Diseases https://www.niddk.nih.gov/health-information/digestive-diseases/crohns-disease/all-content
[7] M. H. Mueller, M. E. Kreis, M. L. Gross, H. D. Becker, T. T. Zittel, and E. C. Jehle, “Anorectal functional disorders in the absence of anorectal inflammation in patients with Crohn’s disease,” Br. J. Surg., vol. 89, no. 8, pp. 1027–1031, 0 2002, DOI: https://doi.org/10.1046/j.1365-2168.2002.02173.x
[8] D. K. Podolsky, “Inflammatory bowel disease,” N. Engl. J. Med., vol. 347, no. 6, pp. 417–429, 0 2002, DOI: https://doi.org/10.1056/NEJMra020831
[9] “Crohn Disease: Practice Essentials, Background, Pathophysiology,” Nov. 2019, https://emedicine.medscape.com/article/172940-overview
[10] Crohn’s & Colitis Foundation, “Overview of Crohn’s Disease,” Crohn’s & Colitis Foundation https://www.crohnscolitisfoundation.org/what-is-crohns-disease/overview
[11] M. Harbord et al., “The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease,” J. Crohns Colitis, vol. 10, no. 3, pp. 239–254, Mar. 2016, DOI: https://doi.org/10.1093/ecco-jcc/jjv213
[12] G. Trikudanathan, P. G. K. Venkatesh, and U. Navaneethan, “Diagnosis and therapeutic management of extra-intestinal manifestations of inflammatory bowel disease,” Drugs, vol. 72, no. 18, pp. 2333–2349, 0 2012, DOI: https://doi.org/10.2165/11638120-000000000-00000
[13] N. Roth et al., “Occurrence of skin manifestations in patients of the Swiss Inflammatory Bowel Disease Cohort Study,” PloS One, vol. 14, no. 1, p. e0210436, 2019, DOI: https://doi.org/10.1371/journal.pone.0210436
[14] B. Thrash, M. Patel, K. R. Shah, C. R. Boland, and A. Menter, “Cutaneous manifestations of gastrointestinal disease: part II,” J. Am. Acad. Dermatol., vol. 68, no. 2, p. 211.e1–33; quiz 244–246, Feb. 2013, DOI: https://doi.org/10.1016/j.jaad.2012.10.036
[15] “Crohn’s Disease : Epilepsy.com/Professionals,” Aug. 05, 2007 https://web.archive.org/web/20070805041654/http://professionals.epilepsy.com/page/inflammatory_crohn.html
[16] W. A. Bye, T. M. Nguyen, C. E. Parker, V. Jairath, and J. E. East, “Strategies for detecting colon cancer in patients with inflammatory bowel disease,” Cochrane Database Syst. Rev., vol. 9, p. CD000279, 18 2017, DOI: https://doi.org/10.1002/14651858.CD000279.pub4
[17] A. Ekbom, C. Helmick, M. Zack, and H. O. Adami, “Increased risk of large-bowel cancer in Crohn’s disease with colonic involvement,” Lancet Lond. Engl., vol. 336, no. 8711, pp. 357–359, 0 1990, DOI: https://doi.org/10.1016/0140-6736(90)91889-i
[18] K. Gerasimidis, P. McGrogan, and C. A. Edwards, “The aetiology and impact of malnutrition in paediatric inflammatory bowel disease,” J. Hum. Nutr. Diet. Off. J. Br. Diet. Assoc., vol. 24, no. 4, pp. 313–326, 0 2011, DOI: https://doi.org/10.1111/j.1365-277X.2011.01171.x
[19] M. C. E. Lomer, “Dietary and nutritional considerations for inflammatory bowel disease,” Proc. Nutr. Soc., vol. 70, no. 3, pp. 329–335, 0 2011, DOI: https://doi.org/10.1017/S0029665111000097
[20] J. H. Cho and S. R. Brant, “Recent insights into the genetics of inflammatory bowel disease,” Gastroenterology, vol. 140, no. 6, pp. 1704–1712, May 2011, DOI: https://doi.org/10.1053/j.gastro.2011.02.046
[21] R. Dessein, M. Chamaillard, and S. Danese, “Innate immunity in Crohn’s disease: the reverse side of the medal,” J. Clin. Gastroenterol., vol. 42 Suppl 3 Pt 1, pp. S144-147, Sep. 2008, DOI: https://doi.org/10.1097/MCG.0b013e3181662c90
[22] T. Stefanelli, A. Malesci, A. Repici, S. Vetrano, and S. Danese, “New insights into inflammatory bowel disease pathophysiology: paving the way for novel therapeutic targets,” Curr. Drug Targets, vol. 9, no. 5, pp. 413–418, May 2008, DOI: https://doi.org/10.2174/138945008784221170
[23] H. Braat, M. Peppelenbosch, and D. Hommes, “Immunology of Crohn’s Disease,” Ann. N. Y. Acad. Sci., 2006, DOI: https://doi.org/10.1196/annals.1326.039
[24] L. Henckaerts, C. Figueroa, S. Vermeire, and M. Sans, “The role of genetics in inflammatory bowel disease,” Curr. Drug Targets, vol. 9, no. 5, pp. 361–368, May 2008, DOI: https://doi.org/10.2174/138945008784221161
[25] J. C. Barrett et al., “Genome-wide association defines more than 30 distinct susceptibility loci for Crohn’s disease,” Nat. Genet., vol. 40, no. 8, pp. 955–962, 0 2008, DOI: https://doi.org/10.1038/ng.175
[26] M. Walker and J. A. Murray, “An update in the diagnosis of coeliac disease,” Histopathology, 2011, DOI: https://doi.org/10.1111/j.1365-2559.2010.03680.x
[27] A. Coghlan, “A single gene can either raise or lower Crohn’s disease risk,” New Scientist https://www.newscientist.com/article/single-gene-can-either-raise-lower-crohns-disease-risk/
[28] D. J. B. Marks and A. W. Segal, “Innate immunity in inflammatory bowel disease: a disease hypothesis,” J. Pathol., vol. 214, no. 2, pp. 260–266, 0 2008, DOI: https://doi.org/10.1002/path.2291
[29] D. J. B. Marks et al., “Defective acute inflammation in Crohn’s disease: a clinical investigation,” Lancet Lond. Engl., vol. 367, no. 9511, pp. 668–678, Feb. 2006, DOI: https://doi.org/10.1016/S0140-6736(06)68265-2
[30] G. M. Cobrin and M. T. Abreu, “Defects in mucosal immunity leading to Crohn’s disease,” Immunol. Rev., vol. 206, pp. 277–295, 0 2005, DOI: https://doi.org/10.1111/j.0105-2896.2005.00293.x
[31] C. O. Elson et al., “Monoclonal anti-interleukin 23 reverses active colitis in a T cell-mediated model in mice,” Gastroenterology, vol. 132, no. 7, pp. 2359–2370, Jun. 2007, DOI: https://doi.org/10.1053/j.gastro.2007.03.104
[32] M. Velasquez-Manoff, “The Worm Turns (Published 2008),” The New York Times, Jun. 29, 2008 https://www.nytimes.com/2008/06/29/magazine/29wwln-essay-t.html
[33] J. Carnahan, “3 Surprising Microbial Triggers of Crohn’s Disease,” Dec. 21, 2017 https://www.jillcarnahan.com/2017/12/20/3-surprising-microbial-triggers-crohns-disease/
[34] S. J. Ott et al., “Reduction in diversity of the colonic mucosa associated bacterial microflora in patients with active inflammatory bowel disease,” Gut, vol. 53, no. 5, pp. 685–693, May 2004, DOI: https://doi.org/10.1136/gut.2003.025403
[35] D. N. Frank, A. L. St. Amand, R. A. Feldman, E. C. Boedeker, N. Harpaz, and N. R. Pace, “Molecular-phylogenetic characterization of microbial community imbalances in human inflammatory bowel diseases,” Proc. Natl. Acad. Sci. U. S. A., vol. 104, no. 34, pp. 13780–13785, Aug. 2007, DOI: https://doi.org/10.1073/pnas.0706625104
[36] C. Manichanh et al., “Reduced diversity of faecal microbiota in Crohn’s disease revealed by a metagenomic approach,” Gut, vol. 55, no. 2, pp. 205–211, Feb. 2006, DOI: https://doi.org/10.1136/gut.2005.073817
[37] A. Darfeuille-Michaud et al., “High prevalence of adherent-invasive Escherichia coli associated with ileal mucosa in Crohn’s disease,” Gastroenterology, vol. 127, no. 2, pp. 412–421, 0 2004, DOI: https://doi.org/10.1053/j.gastro.2004.04.061
[38] K. Fetter et al., “The microbiome landscape in pediatric Crohn’s disease and therapeutic implications,” Gut Microbes, vol. 15, no. 2, p. 2247019, DOI: https://doi.org/10.1080/19490976.2023.2247019
[39] D.-Y. Kang et al., “Diagnosis of Crohn’s disease and ulcerative colitis using the microbiome,” BMC Microbiol., vol. 23, no. 1, p. 336, Nov. 2023, DOI: https://doi.org/10.1186/s12866-023-03084-5
[40] S. A. Naser, S. R. Sagramsingh, A. S. Naser, and S. Thanigachalam, “Mycobacterium avium subspecies paratuberculosis causes Crohn’s disease in some inflammatory bowel disease patients,” World J. Gastroenterol., vol. 20, no. 23, pp. 7403–7415, June 2014, DOI: https://doi.org/10.3748/wjg.v20.i23.7403
[41] S. A. Naser and M. T. Collins, “Debate on the lack of evidence of Mycobacterium avium subsp. paratuberculosis in Crohn’s disease,” Inflamm. Bowel Dis., vol. 11, no. 12, p. 1123, 0 2005, DOI: https://doi.org/10.1097/01.mib.0000191609.20713.ea
[42] G. Agrawal, T. J. Borody, and W. Chamberlin, “‘Global warming’ to Mycobacterium avium subspecies paratuberculosis,” Future Microbiol., vol. 9, no. 7, pp. 829–832, 2014, DOI: https://doi.org/10.2217/fmb.14.52
[43] W. Chamberlin, T. J. Borody, and J. Campbell, “Primary treatment of Crohn’s disease: combined antibiotics taking center stage,” Expert Rev. Clin. Immunol., vol. 7, no. 6, pp. 751–760, 0 2011, DOI: https://doi.org/10.1586/eci.11.43
[44] M. L. Scribano and C. Prantera, “Use of antibiotics in the treatment of Crohn’s disease,” World J. Gastroenterol., vol. 19, no. 5, pp. 648–653, Feb. 2013, DOI: https://doi.org/10.3748/wjg.v19.i5.648
[45] M. Baumgart et al., “Culture independent analysis of ileal mucosa reveals a selective increase in invasive Escherichia coli of novel phylogeny relative to depletion of Clostridiales in Crohn’s disease involving the ileum,” ISME J., vol. 1, no. 5, pp. 403–418, Sept. 2007, DOI: https://doi.org/10.1038/ismej.2007.52
[46] M. Sasaki et al., “Invasive Escherichia coli are a feature of Crohn’s disease,” Lab. Investig. J. Tech. Methods Pathol., vol. 87, no. 10, pp. 1042–1054, Oct. 2007, DOI: https://doi.org/10.1038/labinvest.3700661
[47] M. Martinez-Medina et al., “Biofilm formation as a novel phenotypic feature of adherent-invasive Escherichia coli (AIEC),” BMC Microbiol., vol. 9, p. 202, Sept. 2009, DOI: https://doi.org/10.1186/1471-2180-9-202
[48] K. P. Nickerson and C. McDonald, “Crohn’s disease-associated adherent-invasive Escherichia coli adhesion is enhanced by exposure to the ubiquitous dietary polysaccharide maltodextrin,” PloS One, vol. 7, no. 12, p. e52132, 2012, DOI: https://doi.org/10.1371/journal.pone.0052132
[49] H. Yanai, N. Shimizu, S. Nagasaki, N. Mitani, and K. Okita, “Epstein-Barr virus infection of the colon with inflammatory bowel disease,” Am. J. Gastroenterol., vol. 94, no. 6, pp. 1582–1586, June 1999, DOI: https://doi.org/10.1111/j.1572-0241.1999.01148.x
[50] J. L. Ryan et al., “Epstein-Barr virus infection is common in inflamed gastrointestinal mucosa,” Dig. Dis. Sci., vol. 57, no. 7, pp. 1887–1898, July 2012, DOI: https://doi.org/10.1007/s10620-012-2116-5
[51] S. Lapsia, S. Koganti, S. Spadaro, R. Rajapakse, A. Chawla, and S. Bhaduri-McIntosh, “Anti-TNFα therapy for inflammatory bowel diseases is associated with Epstein-Barr virus lytic activation,” J. Med. Virol., vol. 88, no. 2, pp. 312–318, Feb. 2016, DOI: https://doi.org/10.1002/jmv.24331
[52] R. Ciccocioppo et al., “Human cytomegalovirus and Epstein-Barr virus infection in inflammatory bowel disease: need for mucosal viral load measurement,” World J. Gastroenterol., vol. 21, no. 6, pp. 1915–1926, Feb. 2015, DOI: https://doi.org/10.3748/wjg.v21.i6.1915
[53] B. H. Mullish and H. R. Williams, “Clostridium difficile infection and antibiotic-associated diarrhoea,” Clin. Med., vol. 18, no. 3, pp. 237–241, June 2018, DOI: https://doi.org/10.7861/clinmedicine.18-3-237
[54] L. Saidel-Odes, A. Borer, and S. Odes, “Clostridium difficile infection in patients with inflammatory bowel disease,” Ann. Gastroenterol. Q. Publ. Hell. Soc. Gastroenterol., vol. 24, no. 4, pp. 263–270, 2011 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6334067/
[55] B. G. Mitchell and A. Gardner, “Mortality and Clostridium difficile infection: a review,” Antimicrob. Resist. Infect. Control, vol. 1, p. 20, May 2012, DOI: https://doi.org/10.1186/2047-2994-1-20
[56] N. T. Shen et al., “Timely Use of Probiotics in Hospitalized Adults Prevents Clostridium difficile Infection: A Systematic Review With Meta-Regression Analysis,” Gastroenterology, vol. 152, no. 8, pp. 1889-1900.e9, June 2017, DOI: https://doi.org/10.1053/j.gastro.2017.02.003
[57] J. Burisch and P. Munkholm, “Inflammatory bowel disease epidemiology,” Curr. Opin. Gastroenterol., 2013, DOI: https://doi.org/10.1097/MOG.0b013e32836229fb
[58] N. A. Molodecky et al., “Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review.,” Gastroenterology, 2012, DOI: https://doi.org/10.1053/j.gastro.2011.10.001
[59] Ø. Hovde and B. A. Moum, “Epidemiology and clinical course of Crohn’s disease: results from observational studies,” World J. Gastroenterol., vol. 18, no. 15, pp. 1723–1731, Apr. 2012, DOI: https://doi.org/10.3748/wjg.v18.i15.1723
[60] “Crohn’s Disease Symptoms, Diet, Pictures, Drugs, Life Expectancy,” eMedicineHealth https://www.emedicinehealth.com/crohn_disease/article_em.htm
[61] R. Shoda, K. Matsueda, S. Yamato, and N. Umeda, “Epidemiologic analysis of Crohn disease in Japan: increased dietary intake of n-6 polyunsaturated fatty acids and animal protein relates to the increased incidence of Crohn disease in Japan,” Am. J. Clin. Nutr., vol. 63, no. 5, pp. 741–745, May 1996, DOI: https://doi.org/10.1093/ajcn/63.5.741
[62] J. Cosnes, “Tobacco and IBD: relevance in the understanding of disease mechanisms and clinical practice,” Best Pract. Res. Clin. Gastroenterol., vol. 18, no. 3, pp. 481–496, June 2004, DOI: https://doi.org/10.1016/j.bpg.2003.12.003
[63] S. M. Lesko et al., “Evidence for an increased risk of Crohn’s disease in oral contraceptive users,” Gastroenterology, vol. 89, no. 5, pp. 1046–1049, 0 1985, DOI: https://doi.org/10.1016/0016-5085(85)90207-0
[64] F. Shanahan, “Crohn’s disease,” Lancet Lond. Engl., vol. 359, no. 9300, pp. 62–69, 0 2002, DOI: https://doi.org/10.1016/S0140-6736(02)07284-7
[65] J. K. Hou, B. Abraham, and H. El-Serag, “Dietary intake and risk of developing inflammatory bowel disease: a systematic review of the literature,” Am. J. Gastroenterol., vol. 106, no. 4, pp. 563–573, Apr. 2011, DOI: https://doi.org/10.1038/ajg.2011.44
[66] M. Khatri, “Crohn’s Disease,” WebMD https://www.webmd.com/ibd-crohns-disease/crohns-disease/digestive-diseases-crohns-disease
[67] S. B. Hanauer, “Inflammatory bowel disease,” N. Engl. J. Med., vol. 334, no. 13, pp. 841–848, Mar. 1996, DOI: https://doi.org/10.1056/NEJM199603283341307
[68] “Inflammatory bowel disease (IBD) - Diagnosis and treatment - Mayo Clinic” https://www.mayoclinic.org/diseases-conditions/inflammatory-bowel-disease/diagnosis-treatment/drc-20353320
[69] S. R. Jeon, J. Chai, C. Kim, and C. H. Lee, “Current Evidence for the Management of Inflammatory Bowel Diseases Using Fecal Microbiota Transplantation,” Curr. Infect. Dis. Rep., vol. 20, no. 8, p. 21, May 2018, DOI: https://doi.org/10.1007/s11908-018-0627-8
[70] A. N. Levy and J. R. Allegretti, “Insights into the role of fecal microbiota transplantation for the treatment of inflammatory bowel disease,” Ther. Adv. Gastroenterol., vol. 12, Mar. 2019, DOI: https://doi.org/10.1177/1756284819836893
[71] C. Abercrombie, L. Houser, and G. Tetlow, “An Integrative Approach to Crohn’s Disease: Exploring Autoimmunity in the Gut. You and your Healthy Belly- Part 3,” Philadelphia Integrative Medicine, 2016 https://philly-im.com/blog/integrative-approach-crohns-disease-exploring-autoimmunity-gut-healthy-belly-part-3
[72] B. Dr. Lum, “Functional Medicine For Crohn’s & Ulcerative Colitis | Dr. Brian Lum,” drbrianlum, 2020 https://www.drbrianlum.com/crohn-s-ulcerative-colitis
[73] K. Schepker, “To Help Patients with Irritable Bowel, Clinicians Need to ‘DIGIN,’” Holistic Primary Care, Aug. 13, 2018 https://holisticprimarycare.net/topics/chronic-disease/a-functional-medicine-approach-to-ibd-treatment/
[74] D. T. Rubin, A. N. Ananthakrishnan, C. A. Siegel, B. G. Sauer, and M. D. Long, “ACG Clinical Guideline: Ulcerative Colitis in Adults,” Am. J. Gastroenterol., vol. 114, no. 3, pp. 384–413, 2019, DOI: https://doi.org/10.14309/ajg.0000000000000152
[75] K. Gohil and B. Carramusa, “Ulcerative Colitis and Crohn’s Disease,” Pharm. Ther., vol. 39, no. 8, pp. 576–577, Aug. 2014 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4123809/
[76] “IBD vs. Crohn’s disease vs. IBS: Symptoms, diagnosis, and treatment,” Nov. 22, 2018 https://www.medicalnewstoday.com/articles/323778